Inscription / Connexion Nouveau Sujet
Comprendre l'écriture d'une équation de réaction
Bonjour? je voulais vous demander? si pouvez m'aider à compléter cette exercice? car je bloqué depuis un moment. Merci à tous ceux qui m'aideront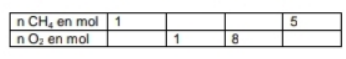
* mmalou > Image recadrée, sur le tableau niquement ! Si tu veux de l'aide, merci de faire l'effort de recopier ton énoncé sur le forum Evie  *
*
Evie, bonjour
merci de lire ![]() [***A LIRE AVANT D'AGIR***] Règles du forum
[***A LIRE AVANT D'AGIR***] Règles du forum
et de t'y conformer en recopiant ton énoncé, ainsi qu'en donnant tes premiers travaux
Bonsoir ! Je suis nouvelle sur le site c'est pour cela que je ne savais pas . Aucun problème je vais recopier l'énoncé et donner mes premiers recherches
Bonsoir. J'aimerai obtenir de l'aide pour mon exercice de chimie sur lequel je bloque. Pour la première colonne je pense que pour l'oxygène c'est 2 car l'atome est présent 2 fois mais c'est tout ce que je sais. Merci à tous ceux qui m'apporteront de l'aide.
*** message déplacé ***
Excusez moi j'ai oublié de mettre l'énoncé.
Le voici :
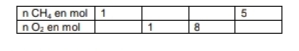
On se place dans les proportions stchiométriques de la combustion du méthane. Reproduire et compléter ce
tableau en conséquence :
On donne : CH4 + 2 O2 CO2 + 2 H2O
*** message déplacé ***
Bonjour,
Ton énoncé semble incomplet : ton tableau correspond bien à des quantités de matière initiales ?
Si tes réactifs sont introduits dans des proportions stoechiométriques, alors tu peux déjà lire l'équation-bilan : CH4 + 2 O2 --> CO2 + 2 H2O
Je lis : pour 1 mole de CH4 réagissant avec 2 moles de O2 il se forme 1 mole de CO2 et 2 moles de H2O
Tu peux alors faire de même avec les valeurs du tableau :
pour ... mole de CH4 réagissant avec 1 moles de O2 il se forme ... mole de CO2 et 1 moles de H2O
pour ... mole de CH4 réagissant avec 8 moles de O2 il se forme ... moles de CO2 et 8 moles de H2O
pour 5 moles de CH4 réagissant avec ... moles de O2 il se forme 5 moles de CO2 et ... moles de H2O
Hélas non, tu ne respectes pas du tout les proportions ...
Si tes réactifs sont introduits dans des proportions stoechiométriques, alors tu peux déjà lire l'équation-bilan : CH4 + 2 O2 --> CO2 + 2 H2O
Je lis : pour 1 mole de CH4 réagissant avec 2 moles de O2 il se forme 1 mole de CO2 et 2 moles de H2O
On va prendre un exemple plus simple :
pour 2 mole de CH4 réagissant avec ... moles de O2 il se forme ... moles de CO2 et ... moles de H2O



