Inscription / Connexion Nouveau Sujet
combustion complete du butane dm
bonjour tout le monde je n'arrive pas a faire un exercice de chimie:
Une bouteille de BUTAGAZ contien m= 13 kg de butane, de formule C[/sub]4H[sub]10.On etudie la combustion complete du butane.
1.ecricre l'equation de la combustion complete du butane.
2.calculer la quantité de matiere initiale de butane.
3.dresser le tableau d'avancement.
4.determiner la quantité minimale de dioxygene necessaire a cette combustion.
5.en deduire le volume de dioxygéne puis le volume d'air dans les conditions de la reaction avec un volume molaire Vm= 24L/mol
6.determiner la masse d'eau obtenue.
7.determiner le volume de dioxyde de carbone obtenu.
8.justifier la presence obligatoire de bouche d'aeration dans toute piece ou se deroule cette transformation.
bien sur je ne veux pas qu'on fasse l'exercice a ma place je veux juste de l'aide pour m'aider a commencer et pour les difficulté que je rencontreraient par la suite.
merci beaucoup!
l'équation est simple
C4H10 + 13/2 O2 donne 4CO2 + 5H2O
et les autres question réflichis bien
merci j'avais trouvé la 1ere question mais pour la 2eme est ce qu'il faut que je fasse masse/masse molaire?
salut,
mais c'est ce que j'ai fais 13000g/58.0
sa me donne environ 224 mol
ok merci ben je vais continuer si j'ai un probleme je reviendrai merci beaucoup de m'aider.
rebonjour excuse moi pourrais tu m'aider pour le tableau d'avancement je melange tout...merci
pou le tableau tu désine deux coulone l'une pou les réactifs et l'autre pour les produits en fonction de temps t=0 puis, t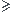 0 est t=fin
0 est t=fin
essaye encore
bon courage


