Inscription / Connexion Nouveau Sujet
TP de chimie
Bonjour à tous !
Voilà je m'adresse à vous en espérant pouvoir obtenir un peu d'aide.
Je dois finir un TP de chimie pour mardi : Bilan de matière: Réaction entre les ions cuivres et hydroxyde
- On a une solution d'hydroxyde de sodium C = 1,0 mol/L et une solution de sulfate de cuivre C = 0,05 mol/L
- Chaque groupe prélève 50mL de la solution de sulfate de cuivre à l'aide d'une éprouvette et le verse dans un bécher
- Chaque groupe recueille dans un bécher un volume différent V de la solution d'hydroxyde de sodium contenue dans la burette puis la verse dans celui qui contient le sulfate de cuivre
- Agiter le mélange avec une baguette et laisser reposer
Gr 1 V = 2,0 mL
Gr 2 V= 3,0 mL ...jusqu'à Gr 9 = 8,0 mL
- Filtrer le contenu de chaque bécher à l'aide d'un entonnoir et d'un papier filtre. Introduisez quelques mL de chaque filtrat dans 2 tubes à essais
- La présence des ions cuivres et hydroxyde sera identifiée à l'aide des deux tests suivants:
- tube 1 : versez quelques gouttes de solution d'hydroxyde de sodiumµ
- tube 2 : versez quelques gouttes de sulfate de cuivre
Pour chaque groupe déduisez si il reste un des réactifs dans le système final
C'est à partir de là que je dois continuer :
1- Ecrivez l'équation chimique traduisant la transformation étudiée dans ce TP:
C'est donc Cu2+ + 2OH- Cu(OH)2
2- Quels sont les groupes où les réactifs ont été entièrement consommés ? Il faudra noter les quantités initiales des réactifs.
Ma prof m'a dit qu'il fallait le prouver par les calculs mais je ne sais pas du tout comment je dois faire.
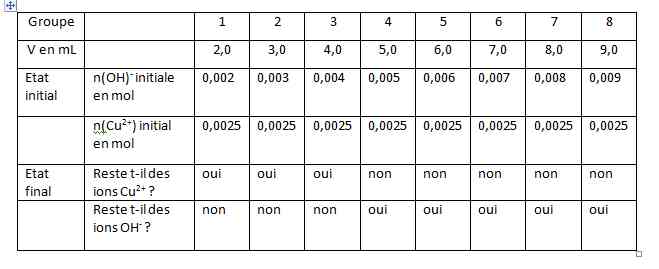
Voilà le tableau qui est donné en dessous que j'ai rempli voir en bas
Quantité de matière du sulfate de cuivre n = C x V
n = 0,005x0,005 = 0,0025 mol
- Retrouver dans le tableau le groupe pour lequel les 2 réactifs ont complètement disparus. Quelles sont les quantités de matière initiales ? Les valeurs obtenues sont-elles cohérentes avec les nombres stchiométriques ?
- Interprétez les résultats des autres groupes
Merci de m'éclaircir un peu 
Salut!
Tu sais faire un tableau d'avancement?
Quoique la relation n = C.V suffit amplement
Sers-toi du tableau complété. Quand tu n'as ni ions cuivrique ni ion hydroxyde à l'état final, c'est que les réactifs ont été consommés... Ici vérifie tes calculs car il doit bien y avoir des groupes pour lesquels ça fonctionne...



