Inscription / Connexion Nouveau Sujet
Titrage d'un produit pour lentilles de contact
L'eau oxygénée, ou solution de peroxyde d'hydrogène H202, est utilisée depuis plus d'un siècle pour ses propriétés antiseptiques dues au dégagement de dioxygène lors de sa décomposition. Sur l'étiquette d'un produit d'entretien pour lentilles de contact, on peut Lire:
« Solution commerciale de décontamination :
- peroxyde d'hydroqène stabilisé: 3,10 g
- eau purifiée ajoutée pour arriver à un volume total de solution de 100 mL. »
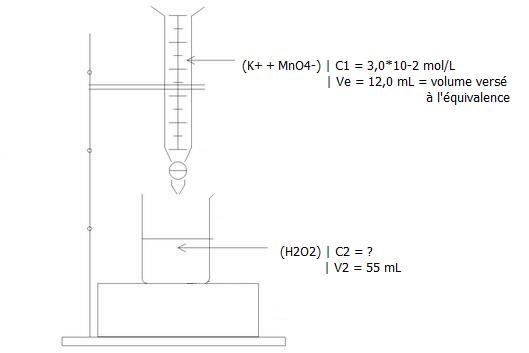
On veut contrôler l'indication de l'étiquette en titrant La solution commerciale diluée par une solution de permanganate de potassium, de concentration en soluté apporté 3,00.10-2 mol.L-1.
1. A partir de la solution commerciale, on prépare 100,0 mL d'une solution S diluée 10 fois. Décrire le protocole de dilution en précisant la verrerie utilisée.
2. Puis, dans un erlenmeyer, on introduit:
- VS = 10,0 mL de la solution S ;
- 5 mL d'une solution d'acide sulfurique concentré;
- 40 mL d'eau distillée;
- un barreau aimanté.
2.a. Faire un schéma du dispositif de titrage.
2.b. Préciser, en le justifiant, avec quel matériel sont prélevés:
- les 10,0 mL de S ;
- les 5 mL d'acide sulfurique ;
- les 40 mL d'eau.
2.c. Quelle est l'espèce titrée ? L'espèce titrante?
3.a. Écrire l'équation de titrage.
3.b. Construire, à l'équivalence E, le tableau descriptif de l'évolution du système.
3.c. Établir la relation entre la quantité initiale en peroxyde d'hydrogène, n(H202,initial) dans le prélèvement de S et la quantité de matière de réactif titrant versé à l'équivalence, n(réactif titrant, versé à E) .
4. Le volume versé à l'équivalence est de 12,0 mL.
4.a. Comment l'équivalence est-elle repérée?
4.b. Calculer n(H202,initial) .
4.c. En déduire la concentration en soluté apporté Cs de la solution S, puis celle de la solution commerciale Co
4.d.. La concentration C0 est-elle en accord avec les indications de l'étiquette ?
Données : Les couples mis en jeu lors de la réaction de titrage sont : MnO4-(aq) / Mn2+(aq) ; 02 (g) /H202(aq)
Bonjour, je suis élève de 1ère S et j'ai un DM de physique-chimie pour les vacances, j'ai besoin d'aides pour cet exercice, je ne comprend vraiment pas grand chose au titrage!

Pour la question 1. et 2. je pense que ca va.
Pour la 2.c. voici ma réponse :
solution titré : H2O2
solution titrante : permanganate de potassium KMnO4
3.a. c'est une réaction d'oxydo-réduction avec les couples qui sont dans les "données", je peux donc déduire :
MnO4- + 8H+ + 5e- = Mn2+ + 4H2O
O2 + 2H+ + 2e- = H2O2
je multiplie les ligne ( par 2 et l'autre par 5 ) pour avoir autant d'électrons dans chaque équations
On a donc :
2MnO4- + 16H+ + 5H2O2 = 5O2 + 10H+ + 2Mn2+ + 8H2O
Jusque là, est ce correct ?
3.b. Ensuite, c'est ici que je bloque et j'ai du mal à comprendre,
A l'équivalence, n(réactif titrant)=0 , oui ?
donc à l'équivalence, n(2MnO4-)=0
Ici, je ne comprend pas ce qu'il faut faire, si quelqu'un peut m'aider ...

Bonjour,
1. A partir de la solution commerciale, on prépare 100,0 mL d'une solution S diluée 10 fois. Décrire le protocole de dilution en précisant la verrerie utilisée.
-> on prélève 10 mL de la solution commerciale qu'on introduit dans une fiole jaugée de 100 mL. On remplit la fiole d'eau distillée jusqu'au trait de jauge. On mélange pour homogénéiser la solution : c'est prêt !
2. Puis, dans un erlenmeyer, on introduit:
- VS = 10,0 mL de la solution S ;
- 5 mL d'une solution d'acide sulfurique concentré;
- 40 mL d'eau distillée;
- un barreau aimanté.
2.a. Faire un schéma du dispositif de titrage. (voir schéma)
2.b. Préciser, en le justifiant, avec quel matériel sont prélevés:
- les 10,0 mL de S ; -> pipette jaugée de 10,0 mL
- les 5 mL d'acide sulfurique -> pipette jaugée (attention c'est dangeraux !)
- les 40 mL d'eau -> avec une éprouvette par exemple.
2.c. Quelle est l'espèce titrée ? -> solution S + acide + eau
L'espèce titrante? -> permanganate de potassium.
3.a. Écrire l'équation de titrage.
Les couples en jeu sont
MnO4- + 8H+ + 5e- = Mn2+ + 4H2O x2
H2O2 = O2 + 2H+ + 2e- x5
___________________________________
2MnO4- + 16H+ + 5H2O2 = 5O2 + 10H+ + 2Mn2+ + 8H2O
donc
2MnO4- + 6H+ + 5H2O2 = 5O2 + 2Mn2+ + 8H2O OUI TB !
3.b. Construire, à l'équivalence E, le tableau descriptif de l'évolution du système.
je te laisse le faire
3.c. Établir la relation entre la quantité initiale en peroxyde d'hydrogène, n(H202,initial) dans le prélèvement de S et la quantité de matière de réactif titrant versé à l'équivalence, n(réactif titrant, versé à E) . -> se déduit du tableau
4. Le volume versé à l'équivalence est de 12,0 mL.
4.a. Comment l'équivalence est-elle repérée?
-> le permanganate de potassium est violet. L'équivalence est atteinte quand il y a décoloration de la solution i.e apparition de Mn2+.
Ensuite il s'agit de la même histoire. Pour retrouver la solution commerciale il faudra multiplier la concentration trouvée par 10. 
4.b. Calculer n(H202,initial) .
4.c. En déduire la concentration en soluté apporté Cs de la solution S, puis celle de la solution commerciale Co
4.d.. La concentration C0 est-elle en accord avec les indications de l'étiquette
Merci ! Mais a la 3.c. je ne comprend pas comment peut on déduire cela du tableau ?
Dans le tableau on sait juste que à l'équivalence n(2MnO4-)=0
Je comprend vraiment pas cette partie je vois pas ce qu'on peut en faire ...
comment peut on trouver la quantité de matière ( initial ou a l'équivalence ) de tout les éléments ?? ( pour remplir le tableau )
et pour la 4.b. comment peut on trouver la quantité de matière ? O_o
n=c*v on n'a pas la concentration
n=m/M on n'a pas la masse
??
oui mais le soucis c'est que je ne retombe pas du tout sur ce qui a écrit sur l'étiquette du fabriquant ... ?!
Je reprends vite fait à partir de 4.
a. Le permanganate est violet. Il est introduit dans le bécher et réagit aussitôt avec H2O2 pour donner MN2+ espèce incolore. A l'équivalence, la solution du bécher devient instantanément violette.
b. n(H2O2) initiale se calcule à partir des données initiales.
c.
2MnO4- + 6H+ + 5H2O2 = 5O2 + 2Mn2+ + 8H2O
L'équivalence est atteinte quand les réactifs de la réaction du dosage ont été introduits dans des proportions stoechimétriques.
On a donc,
n(H2O2) dans V2 / 5 = n(MnO4-) dans Ve /2
<=> C2*V2/5 = C1*Ve/2
<=> C2 = .......
Tu connais maintenant la concentration de H2O2 dans le volume prélevé.
Tu peux donc trouver la concentration de H2O2 dans la solution commerciale
Merci je vais essayer comme ca !
Sinon moi , j'avais déduit ca du tableau :
n(H2O2) - 5xeq = n(MnO4-) -2xeq
n(H2O2) = Veq [ MnO4- ] + 3 xeq
n(H2O2)= m/M = 0,31/34 = 0.009 mol
C2 = 5*C1*Ve / 2V2
C2 = 5*3*10-2*12*10-3 / 2*55*10-3 = 0.016 Mol.L-1
donc on devrais trouvé 0.16 Mol.L-1
mais,
Concentration du fabriquant :
n = m/M = 3.1/34 = 0.091 Mol
c = n/v = 0.091/0.1 = 0.91 Mol.L-1
ah je crois que j'ai compris, pour V2 il faut pas prendre 55e-3 il faut prendre 10e-3 et là je tombe sur 0.9 mol.L-1 a la fin, ca doit etre ca =p
C'est faux. Lors d'une dilution, la concentration de l'espèce diminue mais pas sa masse.
Je te rappelle qu'il y a conservation de la quantité de matière. Souviens- toi du diction "solution mère, solution fille"
Pour 3,1 g de H2O2 dilué dans 100 mL d'eau donne une concentration pour la solution commerciale de
C = 0,91 mol/L
Avec le dosage, on trouve pour la solution dosée
C2 = 1,64*10-2 mol/L
soit C = 0,16 mol/L
C'est que la concentration n'est pas en accord avec l'étiquette.
Oui en fait c'est l'ajout d'eau qui pose pb en fait il y a 2 dilutions.
Il faut adopter le principe solution mère - solution fille pour arriver au résultat.
ah.... et je comprend rien moi au titrage, on a un remplaçant depuis pas mal de temps et je comprend rien avec lui, on a même pas de cours sur le titrage d'ailleurs ... et j'ai 4 autre exercices comme ca a faire en chimie, et autant en physique, demain je part en vacance, enfin bref ... j'ai compris la note quoi.
C'est idiot de rajouter de l'eau ça vous induit à l'erreur.
On va faire comme cela : prend pour V2 le volume prélévé i.e 10 mL.
Dans ce cas comme tu l'as dis plus haut ça marche 
Une personne avait déjà fait cet exo sauf qu'il n'y avait pas 40 mL d'eau à ajouter :
![]() dosage de l eau oxygénée
dosage de l eau oxygénée
1. A partir de la solution commerciale, on prépare 100,0 mL d'une solution S diluée 10 fois. Décrire le protocole de dilution en précisant la verrerie utilisée.
-> on prélève 10 mL de la solution commerciale qu'on introduit dans une fiole jaugée de 100 mL. On remplit la fiole d'eau distillée jusqu'au trait de jauge. On mélange pour homogénéiser la solution : c'est prêt !
2. Puis, dans un erlenmeyer, on introduit:
- VS = 10,0 mL de la solution S ;
- 5 mL d'une solution d'acide sulfurique concentré;
- 40 mL d'eau distillée;
- un barreau aimanté.
2.a. Faire un schéma du dispositif de titrage. (voir schéma)
2.b. Préciser, en le justifiant, avec quel matériel sont prélevés:
- les 10,0 mL de S ; -> pipette jaugée de 10,0 mL
- les 5 mL d'acide sulfurique -> pipette jaugée (attention c'est dangereux !) - les 40 mL d'eau -> avec une éprouvette par exemple.
2.c. Quelle est l'espèce titrée ? -> solution S + acide + eau
L'espèce titrante? -> permanganate de potassium.
3.a. Écrire l'équation de titrage.
Les couples en jeu sont
MnO4- + 8H+ + 5e- = Mn2+ + 4H2O x2
H2O2 = O2 + 2H+ + 2e- x5
___________________________________
2MnO4- + 16H+ + 5H2O2 = 5O2 + 10H+ + 2Mn2+ + 8H2O
donc
2MnO4- + 6H+ + 5H2O2 = 5O2 + 2Mn2+ + 8H2O
3. Faire un tableau d'avancement.
4. Le volume versé à l'équivalence est de 12,0 mL.
4.a. Comment l'équivalence est-elle repérée?
Le permanganate est violet. Il est introduit dans le bécher et réagit aussitôt avec H2O2 pour donner MN2+ espèce incolore. A l'équivalence, la solution du bécher devient instantanément violette.
b. n(H2O2) initiale se calcule à partir des données initiales :
Pour m = 3,1 g et M = 34g/mol.
Donc n = m/M = 0,092 mol.
Pour une solution de 100mL la concentration en H2O2 est C = n/V = 0,92 mol/L
c.
L'équivalence est atteinte quand les réactifs de la réaction du dosage ont été introduits dans des proportions stoechimétriques.
On a donc,
n(H2O2) dans V2 / 5 = n(MnO4-) dans Ve /2
<=> C2*V2/5 = C1*Ve/2
<=> C2 = 5*C1*Ve/(2*V2)
C2 = 1,64*10-2 mol/L
Solution mère :
V'2 = 10 mL
C'2 = ?
Solution fille
V2 = 55 mL
C2 = 1,64*10-2 mol/L
L'ajout d'eau ne modifie pas la quantité de matière :
on a donc V'2*C'2 = C2*V2
<=> C'2 = C2*V2/V'2 = 1,64*10-2 *55*10-3 / 10*10-3
C'2 = 0,09 mol/L
Finalenment, la concentration en H2O2 dans la solution commerciale est C' = 0,9 mol/L
d. Le résultat trouvé est en accord avec l'étiquette (on avait C = 0,91 mol/L)
Voilà 
Erreur de frappe :
pour 4.b, c'est n=3,1/34 = 0,091 soit C = n/V = 0,91 mol/L
Il faut que tu regarde que ma dernière réponse pour ne pas t'embrouiller.
salut tous le monde je passé par la est j'ai remarqué une erreur enfin je pensse
a la 4)b 0.91 mol/l
mais a la d)on a C'2=0.0902 mol/l et d'un coup comme ca elle passe a 0.902 mol/l y'a un pb la xD
autrement dis 10 fois moin important c'est pas en accord ca
pourrait on m'expliquer svp
merci
oups c'est moi qui est deconné en fait c'2 est la solution dilué 10 fois donc C'=10*C'2 = 0.902 mol/l
desoler pour le com inutile ^^'
Ce n'est rien. Il était possible que je fasse une erreur (ce topic date un peu je ne m'en souviens plus).

salut.J'ai eu la chance de tomber sur ce forum qui correspond exactement à mon dns de physique-chimie et j'aimerais avoir d'autres informations si vous voulez bien.
Pour la question 3b qu'est ce qu'il faut metre dans le tableau descriptif ? l'équation de titrage ? je sais pas du tout faire les tableaux d'avancement ... :s
2MnO4- +6H+ + 5H2O2 = 2Mn2+ + 8H2O + 5O2
Etat Avancement
initial X=0 N1 N2 N3 0 0 0
inter x N1-2x N2-6x N3-5x 2x 8x 5x
final xmax N1-2xmax N2-6xmax N3-5xma 2xma 8xmax 5xmax
Mol xmax 0.02-2xmax 3.10-6xmax 0.09-5xmax 2xmax 8xmax 5xmax
j'obtiens ça pour le tableau, donc la quantité initiale en peroxyde d'hydrogène n(H2O2)= 0.09 mol
et la qté de matière de réactif titrant versé à l'équivalence, n= 0.018 mol
d'après 0.09-5xmax=0
xmax= 0.018
C'est ça, ou je suis complètement à côté de la plaque ? :s
J'obtiens la même chose que toi pour le tableau d'avancement, mais je n'arrive pas à calculer N1,N2 et N3 ....? Peux tu m'expliquer comment tu fais s'il te plaît ? =)
Merci d'avance !
pour avoir les quantité de matière de chacun j'ai mis en place la formule n=m/M
par exemple pour le premier, on sait que la masse est de 3.10g, et tu calcules la Masse molaire de MnO4- 
Enfin tout ça c'est d'après moi, mais je sais pas du tout si j'ai bon jsuis pas rodée en tableaux d'avancement ..



