Inscription / Connexion Nouveau Sujet
thermodynamique : cycle moteur
1) justifie le fait qu'un cycle monotherme ne puisse etre moteur .
2) on considère un système décrivant un cycle moteur ditherme , la machine reçoit de la source s1 a la température T1 et le transfert thermique Q1 , et de la source froide s2 a T2 et Q2.
*) donner le rendement 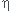 = f(T1,T2)
= f(T1,T2)
*) dans quel sens s'effectuent le transfert thermique
3)quel sont les signes de Q1 , Q2 justifier
4) exprimer la création d'entropie Scrée sur un cycle en fonction Q1 , Q2 ,T1 ,T2
5) déterminer alors le rendement de moteur en fonction T1,T2,Q1,et S crée
non cv je px travailler mais c'est un exercice de DS je vx voir vos essais jé eu 5/20 je comprend pas comment voila 
Bon, voilà ce que j'aurais fait :
1. Un moteur est destiné à fournir du travail à l'extérieur, donc dans un moteur, le fluide reçois un travail négatif : W < 0.
D'après le premier principe, sur un cycle, donc
.
Dans le cas d'un cycle monotherme, le fluide échange de la chaleur avec une seule source de température , donc, d'après l'inégalité de Carnot-Clausius,
donc
ce qui contredit le résultat induit du premier principe, donc il y a impossibilité.
Par conséquent, le moteur monotherme n'existe pas.
2. Dans le cas du moteur ditherme, ,
et
.
A l'aide d'un schéma, il est possible de voir les sens effectifs (ou réels) des transferts d'énergie : le moteur transforme la chaleur donnée par la source chaude en travail et une partie de l'énergie est "perdue" pour l'utilisateur : c'est la chaleur fournie par le fluide à la source froide.
L'énergie utile est ici le travail fourni par le fluide et l'énergie dépensée est la chaleur fournie par la source chaude au fluide.
La rendement du cycle est
or d'après le premier principe de la thermodynamique, pour un cycle,
soit
d'où
Le seul cycle ditherme réversible est le cycle de Carnot (car un échange thermique ne peut être réversible que si , d'où une transformation isotherme ou adiabatique réversible).
Dans le cas général, d'après l'inégalité de Carnot-Clausius,
soit
D'où finalement,
3. J'y ai répondu en début de question 2.
4. C'est immédiat (et ça permet même de démontrer l'inégalité de Carnot-Clausius) :
d'après le second principe de la thermodynamique, pour un cycle,
avec
par définition, donc
.
Comme puisqu'on a un système fermé en contact avec deux sources de chaleur)
on a alors
ou encore
5. Pour voir si tu as compris, je te laisse finir et conclure 


