Inscription / Connexion Nouveau Sujet
thermo.
Bonsoir,
Que vaut le travail W lors dune transformation quasi statique isotherme (de A vers B) ?
Bonsoir.
La question me semble un peu vague.
S'il s'agit d'un gaz parfait : dU=dW+dQ=0 (1ère loi de Joule) => dW=-dQ
Je précise:
Si la transformation de deux moles d'oxygène (supposé être un gaz parfait) passe d'un volume Va à un volume Vb de manière isotherme (A(Pa,Ta,Va);B(Pb=3Pa,Ta,Vb))
Pour calculer le travail en fonction de R et T.
je pars donc du fait que Ta=Tb=PaVa/(nR)=PbVb/(nR)
Puis j'écris W=-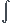 PdV . Et c'est la que je ne sais plus trop ce qu'il faut intégrer (selon l'exercice si c'est isobare isochore, isotherme).
PdV . Et c'est la que je ne sais plus trop ce qu'il faut intégrer (selon l'exercice si c'est isobare isochore, isotherme).
Ici on a un gaz parfait : -pdV = -nRT((dV)/V) et on peut intégrer car on est à température constante


