Inscription / Connexion Nouveau Sujet
Tableau d'avancement
Bonjour à tous,
Alors voilà j'ai cet exercice à faire pour la rentrée et j'aimerais savoir si ce que j'ai fais est bon.
Merci.
Exercice:
Une solution incolore d'acide oxalique, de formule H2C204(aq) est mélangée a une solution de permanganate de potassium qui est violette, dans un milieu acide. l'ion permanganate est la seule espèce colorée du système étudié de formule MnO4(aq), elle est violette.
Initialement, on a mélangé 20.0ml de solution d'acide oxalique de concentration 0.50mol/l avec 5.0ml d'une solution acidifiée de permanganate de potassium de concentration 0.40mol/l en ion permanganate. L'acide est en excès et l'eau constitue le solvant de la solution.
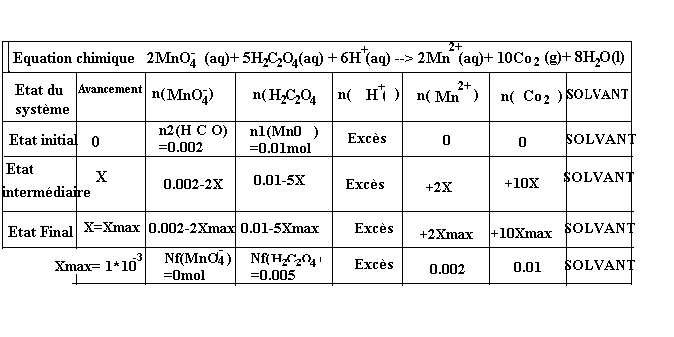
Voici le tableau d'avancement.
2/ Calculer les quantités initiales d'acide oxalique et de permanganate de potassium en mol.
3) Compléter littéralement le tableau d'avancement pui déterminer quel est le réactif limitant.
4/ Justifier que la couleur finale prise par la solution est juste par rapport au réactif limitant.
Réponse:
2/Pour l'acide oxalique:
N(i)1=C1*V1
=0.50*0.020
=0.01 moL ou 1*10-2 mol
Pour le permanganate de potassium:
N(i)2=C2*V2
=0.40*0.005
*0.002 mol ou 2*10-3
3/Si l'acide oxalique est le réactif limitant alors ni(MnO-4)-2Xmax=0
Soit 0.01-2Xmax=0
2Xmax=0.01
Xmax= 2*10-3
Si le permanganate de potassoum est le réactif limitant alors ni(H2C2O4)-5Xmax=0
Soit 0.002-5Xmax=0
5Xmax=0.002
Xmax=1*10-3
Donc on en conclut que, le réactif limitant est le permanganate de potassium de formule MnO-4
4/C'est les ions permanganate qui seul sont responsable de la couleur violette au départ .A la fin de l'expérience la solution est incolore et n'est plus violette contrairement au début de l'expérience. Ceci s'explique par le fait que le permanganate de potassium a disparu, c'est le réactif limitant.

 Merci d'en faire autant la prochaine fois !
Merci d'en faire autant la prochaine fois ! 



