Inscription / Connexion Nouveau Sujet
Synthèse du chlorure d'hydrogène
Bonjour! 
On a corrigé un exo en classe .. et il ya une question d'un exercice que je ne comprends pas :
La synthèse directe du chlorure d'hydrogène se fait sous l'action d'une lumière riche en ultraviolets. Cette synthèse permet d'obtenir un produit très pur , mais elle est très couteuse.
H2(g)+cl2(g) 2HCl
2HCl
DOnc .. cette réaction donne deux molécules d'acide cholorydrique ? 
On mélange 10 moles de dihydrogène et 8moles de dichlore.
DOnc, le réactif limitant est le dichlore. Le dihydrogène est introduit en excès. Quand les 8moles de dichlore auront été consommées, il restera 2 moles de dihydrogène.
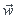 Quelle est la composition du mélange avec réaction ?
Quelle est la composition du mélange avec réaction ?
Ben .. nornalement il ne devrait plus rester de moles de dichlore ?  vu ue les 8moles de dichlore ont été consommées .. Il resterait 2 moles de dihydrogène ..
vu ue les 8moles de dichlore ont été consommées .. Il resterait 2 moles de dihydrogène .. 
Mais je sais que ce n'est pas ça .. Sinon cela reviendrait à écrire : H(2)+CL2  2H
2H
Je ne comprends plus du tout ...
Merci 
On parle plutôt de moles que de molécules, mais c'est un détail. Tu as raison, on obtient bien 2 moles d'acide chlorhydrique si on a 1 mole d'H2 et 1 mole de Cl2 au départ.
Tu as encore raison, on consomme 8 moles de H2, 8 de Cl2. Il va rester 2 moles de H2 et il se sera formé 16 moles de HCl. C'est la composition du mélange obtenu après la réaction.
Merci Physix! 
et .. les 8 moles de H2 et CL2 sont consommées en même temps ? cela va à la même vitesse ?
Pourquoi 16 moles de hcl ?
8H2+8Cl2 16HCl ???
16HCl ???
Merci
Et HCl , c'est ( H2+;cl2) ?
Mais en fait, une solution est électriquement neutre, donc il y a autant d'ions positifs et que négatif. Mais ça ne veut pas forcément dire qu'il faut qu'il y ait la même quantité de matière de H2 et de CL2 ?
HCl, c'est la molécule de chlorure d'hydrogène. Les 2 atomes sont liés l'un à l'autre.
Au contact de l'eau, H et Cl se séparent pour donner deux ions qui ne sont plus liés : H+;Cl-
Lors de la séparation , H perd un électron et Cl le récupère.
Regarde les animations en bas de cette page : ![]()
Ça permet de se faire une idée de se qui se passe même si ce n'est pas tout à fait la réalité.


