Inscription / Connexion Nouveau Sujet
Synthèse de l'acide benzoïque
Bonjour à tous, J'aurais besoin de votre aide, j'ai manqué l'expérience sur la préparation de l'acide benzoïque et je dois répondre aux questions suivantes:
1) A quelle classe appartient l'alcool benzylique ?
2) Ecrire l'équation de dissolution du carbonate de sodium dans l'eau.
3) Ecrire l'équation de réaction acido-basique entre l'ion carbonate et l'eau (qui se comporte en acide).
4) montrer que l'alcool benzylique est légérement en excès dans le mélange réactionnel.
Merci d'avance !!
Bonjour
1) Voici la formule semi-développée de l'alcool benzylique. Est-ce un alcool primaire, secondaire ou tertiaire ?
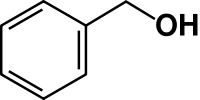
J'aurais besoin d'aide principalement sur la question 4, mon équation d'oxudoréduction étant:
3C6H5-CH2OH+ 4MnO4-  3C6H5-COO- + 4MnO2 +4H2O
3C6H5-COO- + 4MnO2 +4H2O
Je crois que je me suis perdue dans mon tableau d'avancement .
l'énoncé est le suivant:
Protocole: introduire dans le ballon 2,0g de carbonate de sodium Na2CO3, 100mL d'eau, 4,5g de permanganate de potassium et 2,5mL d'alcool benzylique...
Et la question est :
En milieu basique, l'ion permanganate appartient au couple oxydant/réducteur MnO4- / MnO2
La transformation qui a lieu pendant le chauffage est modélisée par l'équation
3C6H5-CH2OH +4MnO4-  3C6H5-COO- +4MnO2+ HO- + 4H2O
3C6H5-COO- +4MnO2+ HO- + 4H2O
Montrer que l'alcool benzylique est en excès dans la mélange réactionnel.
A partir des masses introduites, tu peux en déduire la quantité de matière de chaque réactif. Combien as tu trouvé ? Peux tu me détailler ton tableau d'avancement ?
Pour C6H5- CH2OH, j'ai utilisé n=m/M
Pour m, j'ai utilisé la densité de l'alcool benzylique 1,05*1,00*2,5
et M =108 Donc n= 2,625/108 = 2,4*10-1
Pour le permanganate je bloque
donc n(alcool)=0.24 mol (n'oublies pas l'unité)
POur le permanganate, on l'introduit à l'état solide donc tu peux directement utilsier la formule m=n*M !!


