Inscription / Connexion Nouveau Sujet
Suivi temporel d'une transformation produisant un gaz
Bonsoir a tous, j'ai un DM de chimie plutot difficile, si quelqu'un peut me fournir un peu d'aide merci d'avance!
Enonce:
Une partie du flacon est immergee dans un cristallisoir a temperature ambiante
Le flacon est mis a l'horizontal a t=0 de facon a mettre les reactifs en contact.
L'ordinateur qui joue le role de voltmetre enregistre la tension U a la sortie du pressiometre.
L'equation de la reaction est:
CH3COOH + NaHCO3  CO2 + CH3COO- + Na+ + H2O
CO2 + CH3COO- + Na+ + H2O
La pression dans le ballon est P(ballon)=P(atm) + P où P est la pression due au dioxyde de carbone.
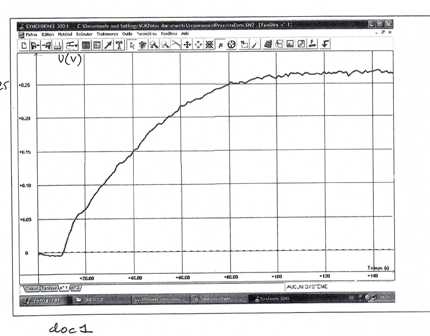
Le systeme d'acquisition est regle de telle sorte que la tension U affichee par l'ordinateur est proportionnelle a P (doc 1).
Questions:
4. la tension U affichee par l'ordinateur est proportionnelle a la pression P due au dioxyde de carbone.
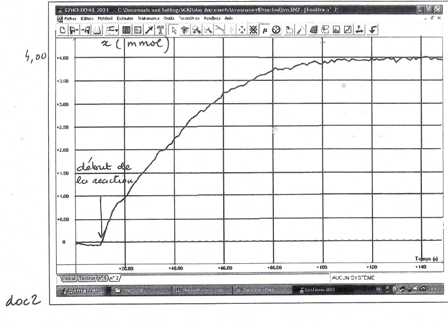
Utiliser la loi des gaz parfaits pour montrer que l'avancement x est proportionnel a la tension U
Determiner a partir du doc 1 U(finale) puis en deduire la valeur du coefficient de proportionnalite entre U et x.
Je n'y comprends rien, toute aide est la bienvenue! Merci
une suggestion
P=kU k constante de proportionnalité
PV=xRT P=xRT/V=kU
U=x*(RT/kV)=x*k' k' étant un terme constant
à la même date ,on peut lire la valeur de x et U
k'=U/x


