Inscription / Connexion Nouveau Sujet
Suivi temporel
Bonjour, pourriez vous m'aider à finir ce TP? Je ne le comprends pas.
On veut suivre l'évolution temporelle de la transformation chimique lente entre les ions I- et les ions S2O82-. Pour cela on réalise des prélevements dans le mélange réactionnele à differentes dates et on titre le diiode formé présent dans le prélevement par une solution titrante contenant des ions S2O32-.
Protocole:
thiosulfate de sodium à c=2,5.10^-2 mol/L dans la burette
mélange d'un volume V1=50mL de iodure de potassium à c1=0,25 mol/L avec un volume V2=50mL d'une solution de péroxodisulfate de sodium ) c2=5,0.10^-2 mol/L.
Prelever et mettre dans des tubes à essai 8 volumes v=10mL de ce mélange réactionnel.
Pour chaque titrage introduire dans un bécher un barreau aimanté et 30mL d'eau glacée + les 10mL de mélange réactionnel. + empois d'amidon.
Déterminer à chaque fois le volume équivalent Véq.
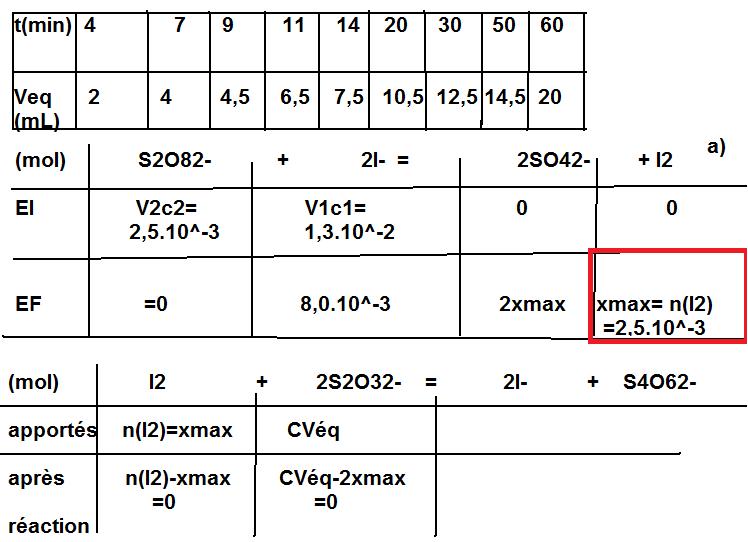
a)A l'aide d'un tableau d'avancement concernant la première réaction (lente), déterminer la relation entre l'avancement xmax et la quantité de matière de diiode n(I2)
b)Déterminer la relation entre l'avancement x et le volume équivalent de la solution de thiosulfate de sodium Veq.
c)Tracer le graphe x= f(t)
d)Justifier la valeur asymptotique de x
e)Déterminer le temps de demi réaction
f)Déterminer les vitesses volumiques de réaction au dates t=0min et t=15min
g)Comment évolue la vitesse volumique de réaction au cours du temps? Comment interpreter cette évolution?
________________________________
a)Je trouve n(I2)=xmax
b)Je trouve n(I2)=xmax donc CVéq =2xmax donc xmax=CVéq*10/2
je fais *10 car on ne prélève que 10mL du mélange réactionnel qui lui a un volume de 100mL
et vous?
c)Quelles échelles choisir?
Je ne comprends pas la question d) et je n'arrive pas à faire celles qui suivent.
Merci de m'aider 
je n'ai pas tout lu ,mais les qtés de matière initiales dans ton tableau sont 10 fois trop grandes.
dans le 100mL de mélange réactionnel
n(I-)= C*v=0,25*0,05=1,3.10-2
n(S2O82-)=0,05*0,05=2,5.10-3
dans chaque tube il n'y a que 10mL du mélange
les qté initiales sont donc divisées par 10
n(I-)= C*v=0,25*0,05=1,3.10-3
n(S2O82-)=0,05*0,05=2,5.10-4mol
recherche du facteur limitant
pour n(I-)-2x=0 x=6,5.10-4mol
n(S2O8)-2)=0 x=2,5.10-4mol
n(S2O8-2) est donc limitant
x(max )=2,5.10-4 mol
comme n(I2)formé )=n((S2O8-2)disparaissant ,n(I2)max=x(max)
en fait les faleurs que tu as noté sont simplement 10 fois trop grandes
je dois m'arrêter pour le moment
dans la question b ,on demande une relation entre l'avancement x et le volume équivalent.
dans le 2ème tableau ,tu as écrit x(max) à la place de x.
En effet ,au bout de 4,7,9 .....min il s'est formé n(I2)=x (x étant de plus en plus grand,jusqu'à atteindre xmax pour une durée très grande )
pour chaque dosage on peut écrire
C*Veq-2x=0
donc x=c*Veq/2
pour chaque date (4,7,.....min)tu peux calculer x
reproupe les résultats dans un tableau
par exemple pour 0 min x=0
pour 60 min x=2,5.10-2*20.10-3/2=2,5.10-4mol
il faut choisir 2 échelles
l'une pour le temps entre 0 et 60 min
l'autre pour x entre 0 et 2,5(*10-4)
Ok mais que répondrais tu à "d)Justifier la valeur asymptotique de x" et "g)Comment interpreter cette évolution?" ? 
la valeur asymtotique c'est xmax.(il ne peut pas se former plus de I2 que xmax)
la vitesses de réaction est proportionnelle à la concentration des réactifs
Au cours de la réaction ,la concentration des réactifs diminue ,donc la vitesse de réaction diminue
Et comment on sait à quelle date on trace la tengente ?
c'est dans l'énoncé
à t=0 et t=15
il y a deux tangentes à tracer



