Inscription / Connexion Nouveau Sujet
représentation du model moléculaire........
voila je voudrais bien savoir si cette représentation des models moleculaires des réactifs et des produits suivant est correcte (type et nombre d'atomes):
1) carbone + dioxygene---->dioxyde de carbone
C + O2------> CO2
2) methane + dioxygene ------> dioxyde de carbone + eau
CH4 + 2O2 ----> CO2 + 2H2O
pour le dernier exemple concernant le butane j'admet que je n'arrive pas a reglé le probleme de l'atome d'oxygene manquant parceque si j'ajoute une melécule de dioxygene j'aurrais un atome d'oxygene en plus 
3) BUTANE + DIOXYGENE ----> dioxyde de carbone + eau
4CH10 + 6O2----> 4CO2 + 5H2O
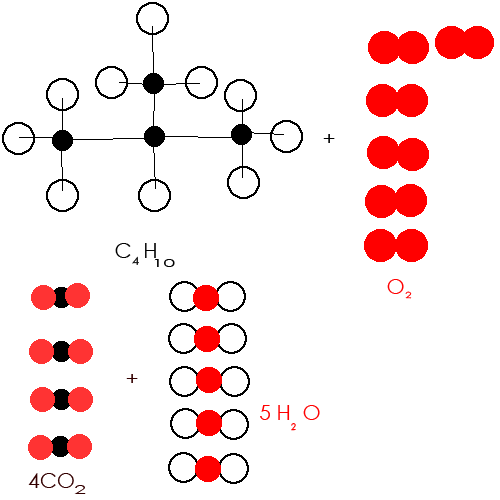
C'est bien pour les 2 premiers mais pour équilibrer la dernière réaction il faut que tu "multiplies" les coefficients par 2 des deux côtés et que tu ajoutes une molécule de dioxygène (O2) en plus !
Ce qui donne :
8 C4H10 + 13 O2 ---> 8 CO2 + 10 H2O
C'est souvent un solution ...
Bonne continuation. A+
je pense que t'as fais une erreur orion dans 8 molecule de butane il n'y a pas 20 atomes d'hydrogene mais plus non?
ce qui signifie que notre équation n'est pas équilibré .
amicalement adel 
Excuse-moi "abdel01", j'ai entré n'importe quoi .... !!!!
Je te donne la bonne équation :
2 C4H10 + 18 O2 ---> 8 CO2 + 10 H2O
Il y a donc du côté des réactifs comme du côté des produits 8 atomes de carbone, 20 atomes d'hydrogène et 36 atomes d'oxygène.
En espérant ne pas m'être une nouvelle fois trompé ... 
A la prochaine 


