Inscription / Connexion Nouveau Sujet
représentation de Lewis molécule H2S
Bonjour pourriez vous m'aider à faire cet exo?
On considère la molécule de sulfure d'hydrogène H2S.
a)Donner la structure électronique des atomes constituant la molécule.
b)En déduire les nombres de doublets d'électrons liants et non liants de la molécule.
c)Combien d'électrons chaque atome doit il engager dans des liaisons covalentes pour satisfaire la règle du duet et de l'octet?
d)Déduire de la question précedente le nombre de doublets non liants de chaque atome.
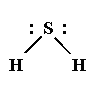
e)Faire la représentation de Lewis de la molécule.
ce que j'ai fait :
a)
1H (K)1
16S (K)4(L)8(M)4
b)Je ne peux qu'en déduire qu'il y aura 4+1+1 = 6 électrons représentés (ce qui ne colle pas avec le reste)
c)Chaque H doit engager 1 électron chacun et S doit en apporter 2.
d)Il y a deux doublets non liants pour S et 0 pour chaque H.
e)
Merci d'avance (surtout pour le question b)) 
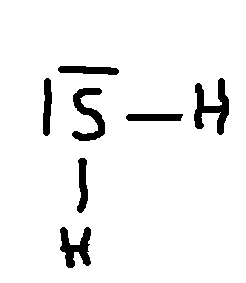
Salut !
!
1) ok pour hydrogène.
Non pour soufre! (K) ne peut être remplies qu'avec deux électrons maxi!
salut aurais tu la correction car je voudrais savoir si j ai juste merci ajoute moi ***
édit Océane : pas d'adresse mail sur le forum, merci