Inscription / Connexion Nouveau Sujet
reaction chimique-equation bilan
bonsoir.Aidez-moi à resoudre ce probleme le voici
1 essence d'automobile a 1 masse volumique 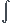 =700kg/m3.on la suppose constituee uniquement d'octane(C[/sub]8H[sub]18
=700kg/m3.on la suppose constituee uniquement d'octane(C[/sub]8H[sub]18
1° ecrire l'equation bilan de la combustion de l'octane ds le moteur de l'automobile en supposant qu'il se forme du dioxyde de carbone et de l'eau.
2° le reservoir d'essence de l'automobile a 1 volume de 50L lorque toute l'essence est consommee
a-calculer la masse de CO[sub][/sub]2 et d'eau rejetee ds l'atmosphere.
b-calculer la masse de d'oxygene consommee.
c-calculer la masse d'air qui a circule dans tubulure du moteur sachant que la composition de l'air est de:80% de dioxyde d'azote et de 20% de d'oxygene .
Bonsoir modzo
1.
Pour avoir des coefficients entiers il sufftit de tout multiplier par 2.
2.
Avec la masse on a:
masse volumique =m/V
=> m= 700 /50*10^3 =0.014 kg=14g
Ceci est donc la masse d'essence qu'on utilise.
On a M(C8H18)=114 g/mol
donc n=1.2*10^-1 mol
donc si la reaction est totale alors on rejette 8*n(C8H18) mol dans l'atmosphere
soit n(CO2)=9.8*10^-1 mol
d'ou m(CO2)=n(CO2)*M(CO2)=43g
b.
A l'equivalence on a:
n(C8H18)=2n(O2)/25
donc n(O2)=25n(C8H18)/2
d'ou n(O2)=1.5mol
d'ou m(O2)=1.5*32=48g
Voila sauf erreur de ma part
Joelz
Bonsoir, je te fais la 1, et tu essayes de faire la suite.
2 C8H18 + 25 O2 -----> 16 CO2 + 18 H2O (à vérifier)
Ensuite tu cherches la masse d'octane dans les 50 litres
puis le nombre de moles d'octane présentes
puis le nombre de moles de CO2 et d'eau rejetées
avec la masse molaire, tu déduis leurs masses.
Même principe pour O2.
Ensuite, compte tenu que dans l'air il y a 20% de O2 tu déduis la masse d'air.
Courage 



