Inscription / Connexion Nouveau Sujet
quotient de réaction; constante d'équilibre
Bonsoir, j'ai des exercices à faire pour les vacances comme entraînement, j'ai la solution de chaque exercice à la fin de mon livre mais je n'arrive pas à trouver le même résultat.
On considère une solution obtenue en dissolvant du nitrate de potassium solide, KNO3(s). On mesure la conductivité de cette solution à 25°C :  =7.24mS.cm-1
=7.24mS.cm-1
1°) Ecrire l'équation de dissolution du nitrate de potassium dans l'eau.
K+(aq) + NO3-(aq) = KNO3(s)
2°) Determiner les valeurs des concentrations des espèces ionique en solution.
Avec pour données: 25°C
 NO3-=7.14mS.m².mol-1
NO3-=7.14mS.m².mol-1
 K+=7.35mS.m².mol-1
K+=7.35mS.m².mol-1
j'ai convertis les données:
 =7.24mS.cm-1= 7.24x10-1 S.m-1
=7.24mS.cm-1= 7.24x10-1 S.m-1
 NO3-=7.14mS.m².mol-1 = 7.14x10-3 S.m².mol-1
NO3-=7.14mS.m².mol-1 = 7.14x10-3 S.m².mol-1
smb]lambda[/smb]K+=7.35mS.m².mol-1 = 7.35x10-3 S.m².mol-&
on sait que  =
=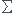 i
i i[Xi]
i[Xi]
Donc [Xi]= /
/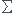 i
i i
i
Alors [NO3-]= 7.24x10-1/7.14x10-3 =101 mol.L-1
[K+]= 7.24x10-1/7.35x10-3 = 98.5
Pourtant le livre me dis que [K+]=[NO3-]=0.05000 mol.l-1
Pouvez vous m'aider s'il vous plaît, je n'arrive à voir ou j'ai faux.
Merci d'avance.
Ceriseuh.


