Inscription / Connexion Nouveau Sujet
Problème liaisons covalentes alcanes
Bonsoir à tous, Physiciens et chimistes !
Alors je vous présente mon soucis.
J'ai du mal à comprendre les liaisons qui soudent un alcane.
Par exemple, je sais que l'atome de carbone (K)²(L)^4 A besoin de 4 électrons pour remplir la sphère extérieure L.
Le méthane CH4 , est un exemple facile à comprendre pour moi , car les Hydrogènes apportent 1 electron de + au carbone en s'associant à lui... Cependant , je ne comprend plus les liaisons carbones et hydrogènes quand le nombre de carbone présent dans l'alcane dépasse 1 !
Par exemple , dans le propane CH3-CH2-CH3 , je ne comprend pas comment le CH2 peut combler sa sphère extérieure, en même temps que les deux CH3.
J'espère que vous avez compris mon problème, ce n'est pas par rapport à la nomenclature des alcènes en elle même, les groupes alkyls, et le nom des alcanes ne me posent pas de problème. C'est ce que moi j'appelle les " liaisons carbone hydrogène " qui me posent problème.
Pour finir, j'ai trouvé un schéma d'une molécule organique ( voir image ) , j'ai entouré la CHOSE qui me pose problème.
Merci de bien vouloir m'aider, en espérant avoir été clair.
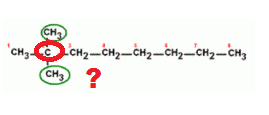
il suffit de retenir le fait que C peut établir 4 liaisons
Quand on écrit CH3 --CH2 --CH3
--représente une liaison C-C ,les indices représentent le nombre de liaisons C-H
si on considère le pemier carbone CH3-- il y a 3 liaisons C-H et une liaison avec le carbone 2. Cela fait bien 4 liaisons
si on considère le deuxième carbone: --CH2-- il y a 2 liaisons C-H ,une liaison avec le carbone 1 et une liaison avec le carbone 3 .Cela fait bien 4 liaisons .
Il me semble avoir compris. Il suffit donc juste qu'il y ai 4 liaisons, que cela soit avec H ou avec C ?
Je vous remercie de votre réponse, car cela me semble plus clair. Mais, je ne comprend pas pourquoi dans l'image que j'ai entouré, il n'y a pas de "H" avec l'atome de carbone.
Merci, bonne soirée.
il n' y a pas de H car ce carbone établit 4 liaisons avec d'autres carbones
Pour t'en convaincre,écris la formule développée ,c'est à dire avec toutes les liaisons C-H.
Tu constateras que chaque carbone est entouré de 4 tirets (=4 liaisons)
Je te remercie. Cependant, j'ai encore une dernière question à te poser.
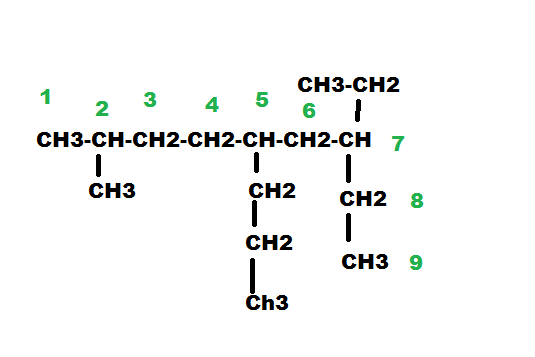
Cette molécule ci-dessous s'appelle le 7-éthyl-2-méthyl-5-propylnonane
Est-ce que la disposition des préfixes, nommant la ramification ( éthyl, méthyl , propyl ) doivent être disposés dans un ordre préçis ?
Ex: à la place de 7-éthyl-2-méthyl-5-propylnonane , peut on écrire : 2-méthyl-5-propyl-7-éthylnonane ?
Ou encore : 5-propyl-2-méthyl-7-éthylnonane ?
Merci, bonne soirée.
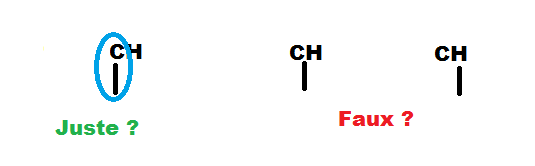
Je ne vois pas la touche "Edit" normalement présente dans tous les forums pour modifier ma question. Je voulais juste m'assurer si quand on dessine un alcane, la liaison doit être sur le C.
on écrit les substituants dans l'ordre alphabétique ,donc éthyl,méthyl,propyl..
le trait part du carbone.C'est donc bien la représentation de gauche qui est juste.
Dans une représentation semi-développée ,on ne matérialise pas les liaisons C-H .Le tiret représente donc une liaison C-C .
![]() Le site a rencontré un problème temporaire.
Le site a rencontré un problème temporaire.
Merci de retenter l'opération plus tard


