Inscription / Connexion Nouveau Sujet
Pression total/partielle Gaz
Bonsoir (: ,
Il s'agit d'un exercice de chimir pour lequel j'ai des difficultés :
Dans un ballon de 5L on mélange 3 gaz à 17°C :
Dioxygène = 4g
Diazote = 28g
Dioxyde de carbone = 5.5g
Donnée: R = 0.082 L.atm-1.K-1.mol-1
1. Calculer la pression totale du mélange
2. Calculer la pression partielle de chaque constituant
1. Tout d'abord je ne trouve aucune formule pour calculer la pression totale du mélange la seule piste que j'ai pu trouver serait PV=nRT
mais la encore pour n je ne sais pas comment faire sachant que j'ai calculer les quantités de matières de chaque constituants.
2. Pour la econde question j'ai besoin de la première question d'ou le soucis.
En vous remerciant d'avance !

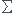 ni !!! Tu peux ainsi en déduire P avec la loi des gaz parfaits !!
ni !!! Tu peux ainsi en déduire P avec la loi des gaz parfaits !!
