Inscription / Connexion Nouveau Sujet
Préparation d'une solution de soude
Bonjour, pouvez-vous m'aider pour cet exo !
L'hydroxyde de soduim NaOH solide fixe facilement la vapeur d'eau présente dans l'air; on dit pour cela qu'il est hydroscopique.Toute solution préparée de NaOh(s) doit donc être étalonnée , puis ajustée à la concentation voulue.
L'objectif est d'aboutir à un volume Vf=100ml d'une solution d'hydroxyde de sodium Sf de concentration molaireCf =0.100mol/l.
1) Premiere étape:
Dans une fiole de 250ml , on dissout 1.10g d'hydroxyde de sodium solide contenu dans un flacon laisser à l'air libre et on complete jusq'au trai de jauge avec de l'eau distilée.On obtient alors la solution de So.
Montrez que cette solution est censé avoir une concentration molaire Co qui dépasse légerement la valeur de Cf.
2) Deuxieme étape :
Pour connaitre précisément la valeur de Co on dilue 10 fois la solution So.Soit S la solution obtenue.
a) Décrivez la préparation de V=100ml de S
b) on intrduit ensuite les 100ml de S dans un bécher, on rince la fiole jaugée et on récupere les eaux de rincage dans le bécher.
A quoi sert cette opération de rincage?
On réalise un dosage conductimétrique de la solution S pour déterminer sa concentration molaire exacte C.
a) le réactif titrant est de l'acide chlorhydrique de concentation molaire
Ca=0.100mol/l . Schématisez le dispositif expérimentale à utiliser sans oublier de légender la figure.
b) Ecrivez l'équation de la réaction de dosage en jeu.
3)Troisieme etape:
La masse d'hydroxyde de soduimutilisée pour préparer So fait que sa concentration dépasse légerement la valeur de Cf . Vous deveez diluer pour obtenir Sf.
a)Quel volume V'o de So devez -vous utiliser?
b) Comment réalisez-vous pratiquement cette préparation de Sf.
Merci d'avance!
1)Utilise no=m/M et Co=no/V soit Co=mo/(M*V)
on a Co>Cf
2) a)méthode classique (à apprendre!)
b)en receuillant l'eau de rinçage ,le bécher contiendra la totalité de la qté de matière de NaOH contenue dans la fiole.
3)question de cours
Une solution de HCl contient les ions H3O+et Cl-
Une solution de NaOH contient les ions Na+ et OH-
l'équation de réaction est celle des ions H3O+ et OH-
3)on veut préparer un volume Vf de solution de concentration Cf,à partir d'une solution de concentration Co (trouvée par dosage)
on calcule le volume Vo à prélever en utilisant le principe de la conservation de la matière.
Co*Vo=Cf*Vf
Le calcul montre que Vo est grand (plus proche de 100mL que de O mL)
on veut Vo+V(eau)=100mL
Au lieu de prélever un volume Vo et de compléter avec de l'eau jusqu'au trait de jauge,on prélève un volume V(eau) à la pipette (V(eau)=100-Vo) et on complète avec la solution So jusqu'au trait de jauge
1) peux-tu me dire si mon résultats est correct
M(NaOH)= 23.0 + 16.0 + 1.0 = 40 g/mol
no=m/M= 1.10/40= 2.75*10^-2
Co = no/(M * V) pour V tu prend Vf=100ml ou pas moi j'ai fait avec .peux-tu me dire si c'est bien ce volume la qui faut prendre?
Co = 2.75*10^-2 / (40 * 0.100)
= 6.87*10^-3
2) a) On prend une fiole jaugée de 200ml , on verse 100ml de la solution S , on ajoute de l'eau distilée puis on agite . Ensuite on réajuste le trait de jauge.
Est ce que il faut faire un calcul avant de décrire ce protocole?
3)b) H3O+/ H2O
H2O / HO-
H3O+ = H2O + H+
HO- + H+ = H2O
ce qui donne l'équation de réaction: HO- + H3O+  2H2O
2H2O
c) que j'ai oubié de mettre .
Il faut en déduire la valeur de la concentration molaire C, puis remontez à celle de Co
Est ce que tu peux m'aider en regardant ce que j'ai fait et me dire si c'est bon!
merci d'avance
est ce que quelqu'un peux me répondre.c'est vraiment urgent je dois le rendre sur feuille à mon prof dans 3 jours. merci d'avance.
l'objectif est de préparer 100mL de solution à 0,100 mol/L
On ne peut pas la préparer directement par pesée car les pastilles de NaOH ont fixé un peu d'eau.
On prépare 250mL d'une solution légèrement plus concentrée que 0,100 mol/l.(C'est la solution So)
On prépare alors 100mL de solution S en diluant 10 fois la solution So
On va doser la solution S.On connaîtra alors sa concentration avec une précision satisfaisante .
On pourra calculer la concentration de la solution So
Co=10*C(s)
on préparera alors 100mL de solution à 0,100mol/L à partir de ce qui reste de la solution So ( une partie des 250 mL aura été utilisée pour préparer S)
vpolà pour le principe de la manip
préparation des 250 mL de solution.
on dissout 1,1 g de NaoH dans 250mL
C=n/V=m/(M*V)=1,1/(40*0,25)=0,11mol/L
pour préparer la 100mL de solution S on doit prélever un volume Vo =10mL de So.
justification
On veut diluer 10 fois So
Co/Cs=Vs/Vo=10 donc Vo=Vs/10=100/10=10mL
En pratique ,on ne prélève pas directement ces 10mL dans la fiole jaugée.(risque de pollution de So).
on verse dans un bécher environ 30mL (c'est à dire un volume suffisant pour pipeter) et on prélève 10mL de cette solution avec une pipette jaugée de 10mL .
on verse ces 10 mL dans une fiole jaugée de 100mL .On complète jusqu'au trait de jauge.On homogénéise par basculement de la fiole bouchée (!)
l'équation est bonne
tu vas pouvoir calculer Cs
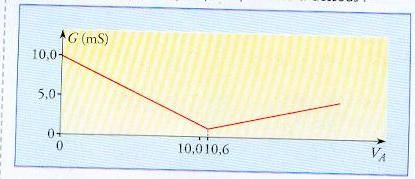
pour la c j'arrive pas à en déduire la valeur de la concentration molaire C, puis remontez à celle de Co . c'est d'apres le graphique que je t'ai mis au dessous.
pourrais - tu m'expliquer .
merci d'avance!
en plus de la question au dessus pourrais - tu me donner ton avis pour la 3eme partie .
a) co * vo = cf * vf
vo = cf * vf / co = 0,100 * 0,100 / 0,110 = 0,100 l
b) f= vo/vf = 0,100 / 0,100 = 1
vf= vo/f= 0,100 / 1 =0,100 c'est pour vérifier
merci d'avance
on dose 100mL de solution s avec une solution de HCl de concentration Ca =0,100mol/L
L'équivalence est atteint quand Va=10,6mL
L'équivalence est atteinte quand les réactifs sont dans les proportions stoechiométriques ( c'est à dire dans les proportions des coefficients des reactifs)
dans ce cas ,l'équivalence est atteinte quand n(OH-)/n(H3O+)=1/1 =1
soit n(OH-)=n(H3O+)
Cs*Vs=CaVa(eq)
Cs=(Ca*Va(eq))/Vs=(0,100*10,6)/100
Cs=0,0106mol/L
C0=10*0,0106
Co=0,106mol/L
A partir de cette solution on veut préparer Vf=100mL de solution de concentration Cf= 0,100mol/L
Co*Vo=Cf*Vf
Vo=(Cf*Vf)/Co
Vo=0,100*100/0,106=94,3mL
plutôt que de prélever 94,3 mL de solution So et de compléter avec de l'eau jusqu'à 100mL,on prélève 5,7mL d'eau que l'on verse dans une fiole jaugée de 100mL et on complète jusqu'au trait de jauge avec la solution So
pourquoi mol/mL?
je ne vois pas de quel résultat tu parles.
S'il s'agit du résultat de Cs=(Ca*Va)/Vs ,
Ca est en mol /L Va et Vs peuvent être exprimés dans n'importe quelle unité pourvu que ce soit la mëme.
Dans ce cas,le rapport Va/Vs est sans unité .Donc Cs a l'unité de Ca c'est à dire mol/L.


