Inscription / Connexion Nouveau Sujet
Nombre de liaison que peut former un atome
Bonjours 
Je voudrais savoir s'il existe une technique pour savoir combien de liaisons pouvait former un atome (par exemple C:4 et O:2) ...
Dans mes souvenirs, très très lointain, il me semble qu'on avait établit la règle du duet et de l'octet mais c'est très flou ! Je me souviens d'avoir déssiné des petites cases avec des points à l'intérieur pour signalé la présence d'un électron ... (après ce n'est qu'un très vague souvenir!)
Donc voilà je vous remercie d'avance !
Bonsoir!
Je te propose de lire ceci : ![]() [lien]
[lien]
Si jamais ça ne te rafraîchit pas la mémoire, je te donnerais des explications plus précises avec plaisir
Alors oui sa m'a bien rafraichit la mémoire merci  mais ... Je ne vois toujours pas !
mais ... Je ne vois toujours pas !
Par exemple prenons le cas de l'oxygène Z=8
Donc K(2) L(6) donc il a 2 electrons internes et 6e- externe situé sur sa couche de valence ... hum ok et ça ne me dit pas le nombre de liaison que peut faire notre petit atome !
Est-ce là ou je dois faire 4 petites case en mettant 1e- dans chaque case et que vu que j'en voi 2 qui forme un doublet électronique donc on aura 2 liaison possible pour l'O .... Pas sure pas sure ! Parce que c'est pas logique si je prend le Bore avec Z=5 si je fais le même résonnement ça veut dire que le bore ne peut faire aucune liaison ...
Alors oui je veux bien des explications si sa ne vous dérange pas! 
Quel est ton niveau? Tu parles de petites cases : cases quantiques? Tu les remplies avec des flèches pour les spins?
Ben à l'époque on appelé pas ça comme ça ... Et je ne suis pas totalement sure que la technique dont je me souviens c'est par rapport aux orbitales ... Je suis en Paces et j'ai un peu honte de plus me souvenir comment on fait !
Ça n'est pas une honte!
En fait tu cherches à faire une sorte de représentation de Lewis, c'est en tout cas le même principe
1) tu comptes les doublets disponibles : Nv,mol = 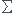 Nv
Nv  charge
charge
+ si la charge est négative et - si elle est positive
Le nombre de doublet s'obtient avec D = Nv,mol/2
2) Utilise les doublets pour former des liaisons et complète l'octet à l'aide de doublets non liants
3) attribue éventuellement les charges formelles
Oui voilà ! et par exemple pour l'atome S par exemple ... J'ai vu en cours qu'il pouvait faire 6 liaisons si ma mémoire est bonne et Mn pouvait en faire 5 ... Pour moi ces deux atomes ne respectent pas la règle du duet ou de l'octet c'est pour ça que j'ai un peu de mal à comprendre ....
Ce sont des exceptions d'après ce que l'on te dit en seconde. Mais en réalité la règle du duet et de l'octet ne marche vraiment que pour les trois premières lignes du tableau périodique des éléments
Hummm d'accord ... Donc je dois faire comment alors pour savoir le nombre de liaison que possède un élement chimique autre que ceux des 3 première lignes du tableau ?
C'est dur à savoir. Le mieux c'est de respecter la méthode que je t'ai donné, sinon on te donnera des indications


