Inscription / Connexion Nouveau Sujet
les acides et les bases
bonsoir,
je suis devant un exercice de chimie :
une solution de HCl de concentration c=1,00 *10^(-8) , son PH = 8.
je n'ai pas accepté que cette solution est basique d'après la définition même si sa concentration est trop faible . le PH doit être <7.
si ce résultat est vrai comment l'expliquer alors qu'on ici un acide fort : donne des protons qui s'ajoute à 10^(-7) de l'eau pure à 25°c.
merci par avance.
Bonjour,
Tu as raison.
Le pH d'une solution de HCl de concentration 1,00.10-8 mol/l n'est pas égal à 8 mais à 6,98
Voir ci dessous les variation de pH d'une solution de HCl pour des concentrations comprises entre 10-6 et 10-8 mol/L
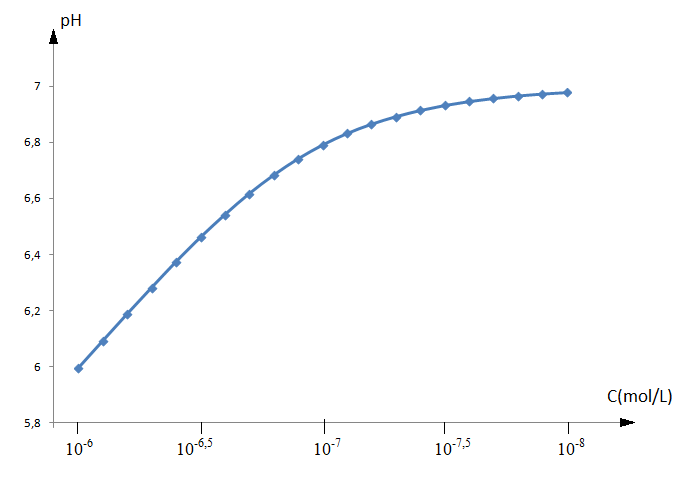
Bonjour et merci
Je voudrais le résultat par les caculs
Ou (pH =- log[H3O+]).
PH= -log(10^(-8)).
Comment s'il vous plait avoir PH de cette solution =6,98 comme l'indique la courbe.
Merci encore
Le calcul "classique" du pH d'une solution de HCl amène à négliger les ions H3O+ provenant de l'eau devant les ions H3O+ amenés par la dissociation des molécules de HCl
On obtient ainsi la relation pH = - log (C0)
Mais cette approximation n'est plus valide pour les valeurs de C0 inférieures à 10-6 mol/L et pour ces valeurs de C0 il est indispensable de tenir compte de l'autoprotolyse de l'eau.
Dans ce cas on est amené à résoudre l'équation [H3O+]² - C0*[H3O+] - Ke = 0,
Cette équation a deux racines, on ne retiendra que celle des racines qui a un sens physique.
On calcule le pH à partir de la solution obtenue pour [H3O+]


