Inscription / Connexion Nouveau Sujet
L'eau Oxygénée
Bonjours, j'ai un devoir maison a rendre pour la fin des vacances mais j'ai un exercice que j'ai commencer mais a la fin je n'y arrive pas je ne sais pas comment calculer, je vous met l'énoncé:
L'eau oxygénée est une solution aqueuse de peroxyde d'hydrogène de formule brute H2O2. On peut la trouver au laboratoire avec l'indication 110 volumes. L'indication "110 volumes" est le titre de l'eau oxygénée ; il exprime le volume de dioxygène (en L et à 0°C et 1 bar) que peut libérer un litre d'eau oxygénée lors de sa décomposition complète en dioxygène gazeux et en eau liquide. On cherche à déterminer la concentration molaire en H202 correspondante. Donnée : à 0°C et 1bar, le volume d'une mole de gza est Vm = 22,4 L/mol(-1).
Questions/reponses:
1.Quelles précautions doit prendre le technicien pour manipuler l'eau oxygénée à 110 volumes ?
Pour manipuler l'eau oxygénée à 110 volumes, le technicien doit éviter de mettre la solution en contact avec sa peau. Selon le pictogramme, le produit est corrosif, il attaque les tissus vivants. Donc pour plus de sécurité, le technicien doit porter des gants mais également une blouse. Dans la question, "quelles précautions" est au pluriel. Pour moi donc les précautions sont d'éviter contact solution-peau et de se protéger avec blouse, gants et lunettes.
2.Écrire l'équation de la réaction.
Équation: 2H2O2 --> 2H20 + 02.
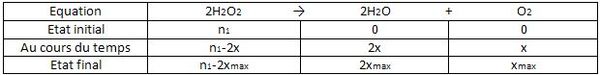
3.Construire le tableau d'évolution.
Je les fait, sur cette questions je ne pense pas mettre trompé
4.Calculer quantité de matière de dioxygène formé lors de la décomposition d'un litre d'eau oxygénée à 110 volumes.
La relation entre quantité de matière n, volume V et volume Vm d'un gaz est : n = V/Vm.
On a V = 110L et Vm = 22,4 L/mol(-1).
Donc n = 110/22,4 = 4,9 mol
Donc quantité de matière n est d'environ 4,9 mol.
5. Déterminer ainsi la quantité de matière de H202 présent dans un litre, puis la concentration en H202.
C'est cette question qui me pose problème. J'ai d'abord calculer quantité de matière avec n = V/Vm puis concentration avec C = n/V. C'est fait. Mais déjà H202 c'est l'eau oxygénée, donc un liquide. Or la relation n = V/Vm n'est que pour les gaz. Je ne sais pas quoi faire?
6.En vous aidant de l'étiquette ci-contre, calculer concentration molaire en H2O2.
Idem, la photo est poster en bas
7.Pourquoi ne retrouve-t-on pas le pictogramme de l'énoncé sur l'étiquette ?
J'aurai dit que la concentration a été "diminué", si c'est sa le terme. Je ne peut pas le justifier sans les questions précédences. Aussi, c'est une forme d'eau oxygénée mise à 10 volumes est un antiseptique, à utiliser sur la peau, donc sur qu'elle n'est pas corrosif ou alors à long terme. et peut être que l'étiquettes est derrières pour un peu d'humour
Merci d'avance de votre aide

Merci de me répondre donc si je suis ton raisonnement, cela fait donc n=V/Vm; mais je voit pas très bien désole mais j'ai quelque difficulté la, si tu pouvais pas juste me donnais une petite aide en plus
merci
Donc si tu détermines x(max) avec ce que tu as trouvé pour le dioxygène, tu peux t'en servir pour le peroxyde d'hydrogène.
Poursuis le raisonnement que tu as entrepris 
Donc je chercherais d'abord xmax, donc n1-2xmax=0 ; xmax=n1/2 ; xmax=4.9/2 ; xmax=2.45 mol
Ensuite j'utilise la formule C=n/v, ce qui donne C=2.45/110=0.0222 mol.L-1
Si c'est sa
Ah c bon enfaîte, je viens de comprendre ma bêtise,n de O2 est 4.9 alors O2 dans la dernière case on met 4.9. Donc Xmax = 4.9, pour H2O2 on calcule : n1 -2 * 4.9 = 0
n1-9.8=0
n1= 9.8 mol
et donc pour la concentration on change juste le nombre, c=9.8/110=0.890 mol.L-1
excusez moi de revenir sur un topic ancien
mais pour la concentration molaire H2O2 à 10 volume
faut faire comment ??
C= ?/10 ?
merci de bien vouloir m'aider
salut  !
!
Tu dois partir de la définition d'une solution à 10 volumes. Qu'est-ce-que cela signifie pour toi ?
salut shadowmiko tu pourrais voir mon nouveau topic sur la relation de conjugaison stp
et m'aider
merci =)
Bonjour , j'up le sujet car j'ai besoin d'aide aussi , donc tout va bien jusqu'a la question 5, après dans cette question pour trouver C , je trouves 0,089 moles et non 0,89 comme l'auteur ...
De plus ma concentration c'est bien mon nombre de mole dans un litre ? Donc la réponse a ma question ?
Pour finir a la q6 , je trouve la meme concentration , 0,089 mol .. C'est normal ?
Bonsoir les amis. Je suis sur le même exercice mais je ne comprends pas l'équation bilan que l'auteur a fait. Pourriez vous me l'expliquer svp . Merci
J'ai maintenant compris bilan. Mais maintenant, au niveau de la question 6, je trouve que la concentration en H2O2 dans 10 volumes est supérieur à la concentration en H2O2 à 100volumes . Est -ce correct? Merci
Bonjour,
Ce sujet est vieux, tu ferais bien de nous détailler tes réflexions pour les questions 1 à 6 pour qu'on puisse regarder ce qu'il en est pour toi.