Inscription / Connexion Nouveau Sujet
iodation de l'acetone
Bonjour a tous !
Je suis en terminale s et j'ai un exercice de chimie a faire pour dans une semaine !
Le problème c'est que je n'arrive pas à repondre à la premiére question ce qui m'empeche de poursuivre l'exercice. J'espere donc que quelqu'un pourra m'aider =)
Exercice :
On se propose d'etudier la cinétique de la reaction du diiode sur l'acetone en presence d'acide chlorhydrique.
Equation
H3C-CO-CH2 + I2 = H3C-CO-CH2I + H+ + I-
Au spectrophotomètre  =350nm et la seule espece absorbante est le diiode.
=350nm et la seule espece absorbante est le diiode.
On etudie 3 solutions :
S1 : 20mL d'acetone à 2.0mol.L-1
10mL d'acide chlorhydrique à 0.10mol.L-1
20mL de diiode à 0.10mol.L-1
S2 : 20mL d'acetone à 1.0mol.L-1
10mL d'acide chlorhydrique à 0.10mol.L-1
20mL de diiode à 0.10mol.L-1
S3 : 20mL d'acetone à 2.0mol.L-1
10mL d'acide chlorhydrique à 0.15mol.L-1
20mL de diiode à 0.10mol.L-1
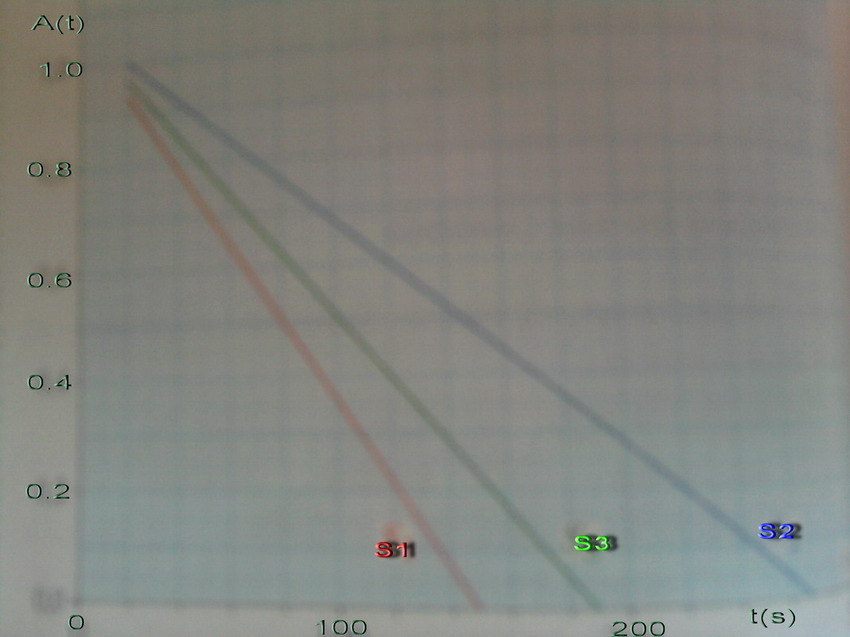
On dispose d'un graphique : A= f(t) et on vois que l'absorbance diminue en premier pour s1 puis s3 et puis pour s2
1 ) Faire un tableau d'avancement et relier l'absorbance de la solution à la composition du système.
soit l'indice i ,pour initial
en cours de réaction
n(acétone)(t)=n(acétone)i -x
n(I2)(t)=n(I2)i -x
donc [I2](t)=n(I2)(t)/Vtotal=(n(I2)1-x)/Vt
on mesure l'absorbance de I2.L'absorbance est proportionnelle à la concentration
A=k*[I2]=k*(n(i2)i-x)/Vtotal
Merci beaucoup , mais je ne comprends pas comment tu sais que A est proportionnel a C
et que représente k ?
Merci beaucoup , mais je ne comprends pas comment tu sais que A est proportionnel a C
et que représente
c'est une propriété de la loi de Beer Lambert
A=
 .l.C
.l.C
A est proportionnelle à l'épaisseur de la solution traversée par la lumière (l),à la concentration C et à
 ,terme qui dépend de la nature de la substance absorbante et de la longueur d'onde.
,terme qui dépend de la nature de la substance absorbante et de la longueur d'onde.
en écrivant A=k*C on exprime le fait que A est proportionnelle à C.
k est le facteur de proportionnalité .k=
 *l.
*l.
Si on construit une courbe A=f(C),la pente de la tangente en tout point de la courbe vaut k.
ah d'accord merci, mais on ne possede pas cette courbe et on ne nous demande pas de la tracer , donc je ne dois pas calculer k?
question 2 : Rappeler la definition de vitesse volumique de reaction. Comment calculer la vitesse volumique de la reaction a partir de la courbe a=f(t)
Voila je ne vois pas de rapport avec la question 1, et pour reailiser le tableau d'avancement , on fait le tableau d'avancement basique ?
ton problème m'embarrasse car pour calculer v en fonction de A ,il faudrait connaître le facteur de proportionnalité entre A et C
par définition
v=(1/V)/dx/dt x étant l'avancement
à un instant t
n(I2)t=n(I2)i -x
x=n(I2)i -n(I2)t
n(I2)i étant une constante,
donc
comme A =k*C,
C=A/k avec C=[I2]
dA/dt est la pente de la tangente en un point du graphe A=f(t)
on peut donc calculer dA/dt pour différents points ,mais il faut la valeur de k pour pour calculer v
On en revient à la question 1.
il faut un moyen de relier A et [I2].
après,il est facile de relier [I2] à x.
regarde bien si dans ton énoncé ,il n' y a pas une information utile (par exemple une valeur de A pour une valeur de [I2]connue.
si non ,j'essaierai de t'orienter vers un autre intervenant
dans mon livre j'ai une aide pour la question 2 : Utiliser A(0) pour determiner l x E CI[sub]2[/sub] en fonction de A(t)
CI[sub]2[/sub] en fonction de A(t)
voila il n'y a rien d'autre
je ne pouvais pas deviner que la décroissance était linéaire ...
d'ordinaire,c'est une exponentielle.
dans ce cas
A=k*t k étant la pente de chaque droite
Ecris ton énoncé en entier ,car je ne peux pas deviner les particularités de cet exercice