Inscription / Connexion Nouveau Sujet
Hugoniot et Bernoulli
bonjour je suis actuellement en PCSI je passe en PC et un exo d'entrainement de mes vacances me laisse perplexe je ne comprends pas vraiment ce qu'on doit obtenir a la question suivante:
Le gaz(regime permanent) recoit de la chaleur et du travail des pales son altitude z est variable: au début une masse m de fluide possède les carac. suivantes ( P1,V1,T1et Z1) et passe a P2 T2 V2 z2 en sortie
Appliquer le 1er principe a M par le biais de l'enthalpie H
Claculer sa cariation d'Energie Meca si le passage début fin se fait réversiblement fonction de W et la primitive de 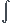 (VdP)
(VdP)
Mon problème est que je ne vois pas exactement a quoi aboutir dans la premiere partie de la question pour l'instant toutes mes recherches auraient pu revenir a recopier stricto census mon cours ce qui ne presente aucun interet d'ou ma demande d'éclaircissement
Merci d'avance
Bonjour
Le seul exemple d'application du premier principe de la thermo à un système ouvert en Sup concerne la détente de Joule-Thomson. Revois bien la démonstration et adapte-là en remplaçant le milieu poreux isolé thermiquement par une machine possédant des parties mobiles (pales...) non isolée thermiquement. En s'intéressant à une masse m de fluide à l'entrée de la machine (état 1) qui ressort de la machine dans un état 2, la démonstration, qui tient compte des éventuelles variations d'énergie potentielle de pesanteur et d'énergie cinétique macroscopique conduit à :
WP représente le travail des forces de pression exercées par le gaz situé en amont et le gaz situé en aval de la machine : WP=P1V1-P2V2 ; d'où l'expression du premier principe valide pour les systèmes ouvert en régime permanent :
où W' représente le travail technique c'est à dire le travail fourni à la masse m de fluide par les parties mobiles de la machine.
Pour de très nombreuses machines (compresseurs, turbines traversées par des gaz) les variations d'énergies cinétique et potentielle macroscopiques sont négligeables, ce qui donne :
Puisqu'on raisonne sur une variation de fonction d'état, on peut calculer cette variation en imaginant une évolution fictive entre l'état initial réel et l'état final réel : on imagine que la masse m de gaz traverse une succession de machines élémentaires. Pour chacune, la relation devient :
Soit en utilisant la seconde identité thermodynamique :
Si l'évolution est réversible, cela se simplifie :
Par intégration entre l'état réel initial et l'état réel final :
Ainsi représente le travail technique dans le cas limite d'une évolution réversible, souvent appelé travail de transvasement. Son calcul dépend du type de fluide et du type de transformation. Si le fluide est assimilable à un gaz parfait, le calcul de l'intégrale n'est souvent pas nécessaire, il suffit d'appliquer au gaz la seconde loi de Joule.


