Inscription / Connexion Nouveau Sujet
formation d'un précipité
salut pouvez vous m'aidez pour cet exercice s'il vous plait merci d'avance.
Dans un tube à essais, on mélange une solution de chlorure de sodium (constituée d'ions sodium Na+(aq) et chlorure Cl-(aq) et une solution nitrate d'argent (constituée d'ions argent Ag+(aq) et nitrate NO-3(aq).
il se forme un précipité blanc qui noircit la lumière.
a.Décrire l'état initial du système.
b.Y a-t-il eu transformation chimique? pourquoi?
c.quel est l'état physique de l'espèce chimique obtenue?
d.Quels sont les réactifs? les produits?
e.Quels sont les ions qui ne participent pas à la réaction?
Bonjour, il faut que tu postes les réponses aux questions !
1. Etat intial :
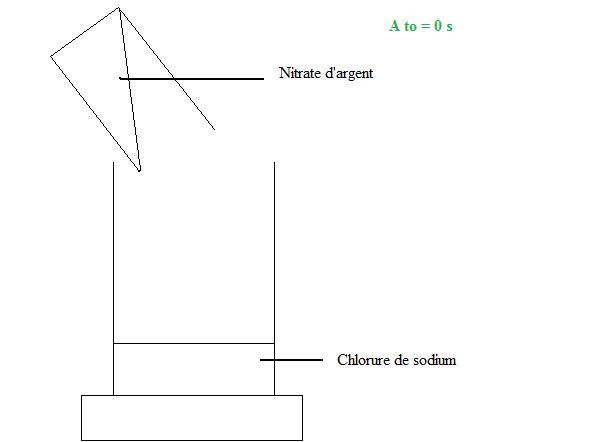
2. Il y a transformation chimique car il y a formation d'un précipité blanc qui noircit à la lumière.
3. L'espèce chimique obtenue est la précipité chlorure d'argent AgCl.
4. Réactifs : Ag+ et Cl-
Produits : AgCl
5. Ions spectateurs : NO3- et Na+
_____________________________________________________________________________________
La prochaine fois chatouille, j'aimerais bien te voir chercher un peu l'exercice. Il n'était pas difficile, il fallait juste bien lire l'énoncé et connaître son cours. 


