Inscription / Connexion Nouveau Sujet
famille et propriétés chimiques
Bonjour tout le monde 
DM de physique :
Le plâtre est essentiellement constitué de sulfate de calcim de formule brute CaSO4, 2H2O. Il est constitué d'ions Ca2+ et d'ions SO2-4.
a. Où se situe le baryum Ba par rapport au calcium dans la classification périodique?
Je sais qu'il est dans la même colonne que le calcium mais je ne sais pas comment expliquer.
(J'attend pour les questions suivantes si jamais j'ai compris ^^)
Merci 
Salut !
!
Connais-tu la règle du duet et de l'octet? Par rapport à ça, que signifie le fait que Ca et a soient ds la même colonne? (utilise le mot famille ds ta réponse)
Ah ok Merci 
b) Donner la formule brute du sulfate de baryum déshydraté. Ce solide peut capter des molécules d'eau ; peut-on prévoir combien par comparaison avec les données de l'énoncé ?
Formule : BaSO4
Oui on peut prévoir (donc il y en a deux car dans l'énoncé il y a marqué 2H2O).
__________
2. a) Dans combien de liaisons covalentes est engagé l'atome d'oxygène dans la molécule d'eau ?
Je sais que les atomes des éléments d'une même colonne forment le même nombre de liaisons covalentes mais là je ne sais pas du tout.
b) Le soufre est sous l'oxygène dans la classification périodique. En déduire la formule de Lewis de l'analogue soufré de la molécule d'eau. C'est le sulsfure d'hydrogène, gaz à odeur nauséabonde.
Et cette question j'y comprend rien  La formule de Lewis je sais faire mais c'est quoi l'analogue soufré de la molécule d'eau ?
La formule de Lewis je sais faire mais c'est quoi l'analogue soufré de la molécule d'eau ? 
Merci 
Re
b) oui mais prq peux-tu le prévoir?
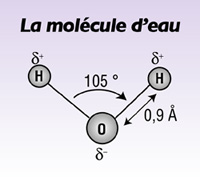
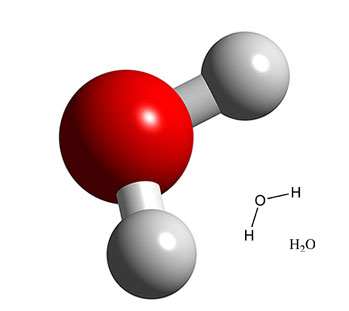
2) a) Ecris la formule de Lewis de la molécule d'eau (coude ta molécule)
Que vaut Z pour O? Z = 8 non? Dc sa strucure électronique est (K)2(L)6. Il lui faut donc capter deux électons pour obtenir une structure stable en octet comme le Néon (Z = 10).
Donc deux liaisons covalentes...
b) H2O = eau. Le S est sous O dans la classification périodique dc il fait parti de la même famille (chalcogènes). Il lui faut donc d'après la question 2)a), deux électrons pour saturer sa couche externe et avoir une structur électronique stable semblable au gaz inerte le plus proche, à savoir l'Argon.
Dc il doit se lier avec deux atomes d'hydrogène, et tu obtiens H2S.
Encore une fois, un très bon moyen de se justifier est de donner les structures électronique et de représenter les formules de Lewis (sans oublier les doublets non-liants). Ces deux molécules présentent une forme coudée
Re 
Merci beaucoup 
Ca veut dire quoi coudé ? 
Voilà ce que j'ai compris ^^ :
2) a) H2O : H(Z=1) = (K)1
O(Z=8) = (K)2(L)6
ne(H) = 1 ne(O) = 6
Pour avoir une couche externe saturé il manque 2 électrons donc 2 liaisons.
b)Comme le soufre est sous l'oxygène, ils sont de la même famille.
Comme il manque 2 éléctrons à l'oxygène pour être stable , il manque aussi 2 électrons au soufre pour être stable. Donc la formule de l'analogue soufré de la molécule d'eau est H2S.
Il faut faire le dessin ou juste donner la formule : H2S ?
2) a) ok
b) ok. Tu peux faire le dessin, ça aide à justifier le fait que ces deux molécules présentent la même allure
molécule d'eau:
Tu remarques qu'elle ressemble à Mickey et qu'elle n'est pas linéaire. Dc elle est coudée.