Inscription / Connexion Nouveau Sujet
Exercide "Dosage des ions fer III"
L'ion fer (II) peut être oxydé par l'ion permanganate en milieu acide. On utilise cette réaction pour doser une solution contenant des ions fer (II).
1) Ecrire l'équation-bilan de la réaction de dosage. On donne les demi-équations électroniques :
Fe(3+) + e- = Fe2+
MnO4(-) + 8H(+) + 5e- = Mn(2+) + 4H2O
j'ai donc ecrit : 5Fe(3+) + Mn(2+) + 4H2O -> 5Fe(2+) + MnO4(-) + 8H(+)
J'aimerais savoir si c'est correct,
et puis ensuite on me demande de montrer qu'il est nécessaire d'acidifier la solution de permanganate pr effectuer ce dosage et je ne sais pas quoi faire :s Qqun peut-il m'aider ?
Tu n'as pas l'air sûre.
Pour la réaction entre la carbone et le dioxygène tu dis bien que
C + O2 -> CO2 non ?
Il est nécéssaire d'ajouter de l'acide sulfurique (2H+ + SO42-) car l'équation de la réaction nous dit qu'elle consomme des ions H+ !
Avec cet exemple, oui je comprends mais pas avec mon équation.
Les ions ferreux réagissent avec les ions permanganate. Or les réactifs se mettent à gauche.
Ton équation est donc 5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2+ + 4H2O
Une derniere question
"on dose 20mL d'une solution contenant les ions fer (II) par une solution de permanganate de concentration 2.0*10^-2mol/L. Le volume de permanganate versé à l'équivalence est Ve = 12.0mL. Calculer la concentration en ions fer (II) de la solution."
Pour ça je fais C1*V1=C2*V2 ???
d'où ça sort il faut toujours expliquer ce que tu fais (en plus ça fait gagner du temps aux correcteurs  )
)
Oh non, je n'y arrive pas  . j'ai calculé n(permanganate) = c*v donc 24*10^-2 est-ce que ça me sert dans mon calcul ?
. j'ai calculé n(permanganate) = c*v donc 24*10^-2 est-ce que ça me sert dans mon calcul ?
Voici une solution bien rédigée :
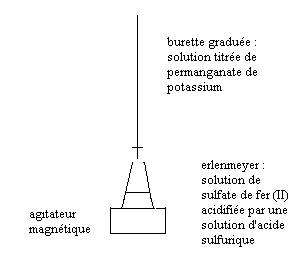
* Schéma annoté du dosage avec
dans le bécher la solution en ions fer (II) de concentration C1= ? et de volume V1=20mL = ... L
dans la burette graduée la solution de permanganate de potassium de concentration C2 = 2.0*10-2mol/L et de volume Ve = 12.0mL = .... L = volume versé à l'équivalence.
* L'équation de la réaction du dosage est :
5Fe2+ + 1MnO4- + 8H+ = 5Fe3+ + Mn2+ + 4H2O
* L'équivalence est atteinte quand les réactifs de la réaction du dosage ont été introduits dans des proportions stoechiométriques.
On a donc
n(Fe2+ dans V1)/5 = n(MnO4- dans Ve)/1 (ce sont les coefficients devant les réactifs dans ton équation)
<=> C1*V1/5 = C2*Ve
<=> C1 = ....... mol/L (attention à bien convertir les volumes en L !) 
ok je vais devoir m'en aller.
Il faut la prochaine fois que tu expliques bien ce que tu fais.
Tu vois avec ma rédaction-type,
on voit ce qu'on fait (le dosage explicité par le schéma)
ce qu'on a (la réaction entre les 2 espèces)
la condition d'équivalence 
tu peux me tutoyer mais bon je te fais confiance pour le petit calcul (il suffit de passer de la formule littérale au calcul) 



