Inscription / Connexion Nouveau Sujet
Exercice Précipitation MgF2
La solubilté de MgF2 = 1.21.10^-3
1/ quel est le produit de solubilté de MgF2?
2/ Une solution contient 0.1 mole par litre d'ions Mg2+ et 1 mole par litre d'ions F. Est elle saturée?
3/ même question avec 10^-4 moles Mg2+ et 10^-2 moles de F par litre
4/ Quelle est la solubilité de MgF2 dans un solution contenant initialement des ions F- de concentration 10^-1 mol/L ?
5/ même question avec une concentration initiale d'ions Mg2+ 10^-1 mol/L
Voici l'énoncé d'un exercice que je n'arrive pas à faire...
Si qqn veut bien m'aider ce serait chouette !
Merci d'avance
Bonsoir,
Commence par écrire l'équation de dissolution de MgF2 :
MgF2 = Mg2+ + 2F-
Le produit de solubilité c'est le Ks :
Ks = [Mg2+]*[F-]² = s * s² = s3
= (1.21.10^-3)3 = 1,77 * 10-9
Ensuite,
La solution est saturée si :
Ks = [Mg2+]*[F-]² (où si le produit des concentrations est supérieure ou égal au Ks)
Or [Mg2+]*[F-]² = 0,1 *(1)² = 0,1 * 1 = 0,1 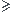 1,77*10-9 = Ks
1,77*10-9 = Ks
la solution est saturée !
Sauf erreur, as-tu compris ? As-tu d'autres questions ?


