Inscription / Connexion Nouveau Sujet
Exercice de physique chimie titrage
Bonjour, excusez-moi de vous déranger mais j'aurais besoin d'aide pour un exercice de Chimie.
Voici l'énoncé :
Le détartrant pour cafetière est vendu sous forme de poudre blanche. Celle-ci est essentiellement constituée d'acide sulfamique de formule H2NSO3H(S). Les solutions de cet acide détruisent les dépôts de calcaire qui se forment dans les cafetières électriques. Sa base conjuguée est l'ion sulfamate H2NSO^- 3(aq).
On dissout 200,0 mg de ce détartrant dans un peu d'eau distillée contenue dans une fiole jaugée de 250,0 mL. On complète avec l'eau distillée jusqu'au trait de jauge puis on agite. On dispose alors d'une solution SA.
Pour doser cette solution SA, on utilise une solution aqueuse d'hydroxyde de sodium Na^+ (aq) + OH^- (aq) (soude) que l'on appellera SB.
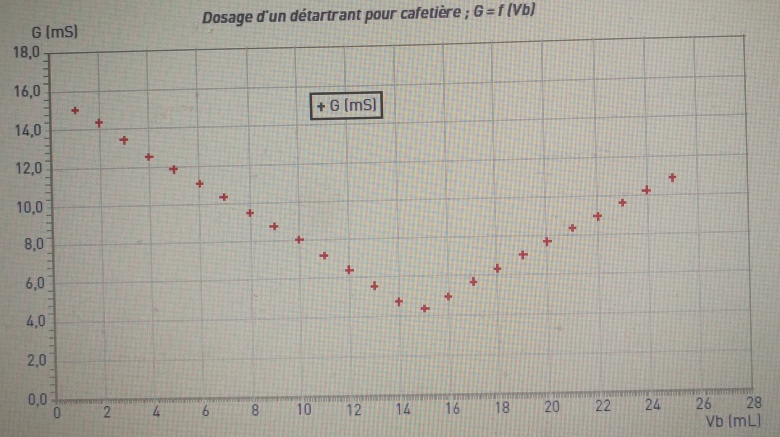
On dose, à l'aide d'une sonde conductimétrique, un volume VA = 20,0 ml de la solution de détartrant SA de concentration CA, par la solution d'hydroxyde de sodium SB, de concentration molaire CB = 1,0.10-2 mol.L-1. La courbe donnant l'évolution de la conductance G en fonction du volume de soude VB ajouté est donnée ci-dessous.
Les questions sont les suivantes:
1. Réaliser un schéma annoté du montage nécessaire pour effectuer ce dosage.
2. Donner l'équation bilan de la réaction du titrage.
3. Définir l'équivalence.
4. Compléter le tableau d'avancement de ce titrage.
5. Déduire de ce tableau la relation entre la concentration molaire CA, le volume VA, la concentration CB
et le volume VB,E de solution SB ajouté à l'équivalence.
6. Déterminer, sur la courbe du titrage, le volume VB,E de solution titrante d'hydroxyde de sodium ajouté
à l'équivalence. (Faire figurer les traits de construction.)
7. Calculer la concentration CA de la solution SA d'acide sulfamique.
8. Calculer la masse mA d'acide sulfamique présent dans la solution SA. En déduire le pourcentage massique de l'acide sulfamique
contenu dans le détartrant.
Ca fait beaucoup mais je bloque complètement... :/
Si quelqu'un pouvait m'aider, ce serait très gentil 
Merci d'avance
Bonsoir,
Les trois premières questions sont des questions de cours qui ne présentent pas d'autre difficulté que de l'avoir appris. ( le cours !)
La question 2 est dispensable pour traiter la question 4 dans laquelle il est question de tableau d'avancement à compléter.
Merci de publier ce tableau ( même non complété ), car il constitue le point de départ de la résolution de l'exercice.
Bonjour
Merci pour votre réponse et excusez moi de répondre si tard.
Pour la question 1, j'ai réussi à faire le schéma.
Pour la question 2 je sais ce qu'est une équation bilan, je pense qu'il faut mettre d'un coté H2NSO3-(aq) et de l'autre NA+(aq) + OH-(aq) ou pas?
J'ai essayé plusieurs fois de joindre le tableau mais je n'y parviens pas donc je vais l'écrire ci dessous:
Avancement (en mol)
Etat initial 0
Etat en cours de
transformation x
Etat final à
l'équivalence xE
Merci d'avance 
Bonjour,
J'ai posté cet énoncé il y a assez longtemps mais personne ne réponds depuis... Comme je sais que c'est interdit de poster deux fois le même sujet, je réecris pour savoir si quelqu'un pouvait m'apporter de l'aide.
Merci d'avance
Tu n'as toujours pas répondu à la question 2 qui est pourtant une question de cours.
Le titrage s'appuie sur une réaction chimique entre la solution SA d'acide sulfamique et les ions HO- présents dans la solution SB d'hydroxyde de sodium.
C'est l'équation de cette réaction qui t'es demandée.
Elle est indispensable à la poursuite de cet exercice.
Je te guiderai très volontiers si tu proposes une réponse.
Bonjour,
Excusez-moi de répondre si tard je viens de rentrer de voyage.
Merci pour votre réponse 
Si "Le titrage s'appuie sur une réaction chimique entre la solution SA d'acide sulfamique et les ions HO- présents dans la solution SB d'hydroxyde de sodium" alors l'équation ressemble à ça :
H2NSO3H(S) -> OH-(aq)
non?
Par contre je ne comprends pas pourquoi du coté gauche on met uniquement l'acide sulfamique et pas la formule de la solution SA avec l'eau distillée)
Merci d'avance
L'acide sulfamique et les ions HO- sont les réactifs.
La réaction est du type "acide-base".
Quels sont les produits obtenus ?
D'accord.
Mais je ne comprends pas car il y a deux solutions dans l'énoncé :
La SA qui est de l'acide sulfamique avec de l'eau distillée et la SB qui est l'hydroxyde de sodium avec la SA.
Si les réactifs sont l'acide sulfamique et les ions hydroxyde alors ca me paraitrait logique si les produits obtenus sont l'eau distillée et les ions Sodium mais je ne suis pas sûre.
Merci
Aïe, aïe, aïe !
Cela ne va pas du tout !
Est il bien raisonnable de chercher à résoudre cet exercice sans même connaître le mécanisme d'une réaction acide/base ?
La réaction qui se produit est l'interaction entre deux couples acide / base
a) Le couple H2NSO3H / H2NSO3-
b) Le couple H2O /HO-
Les ions Na+ qui sont présents dans la solution SB ne participent pas à la réaction et ne figurent pas dans l'équation de la réaction : Ce sont des ions spectateurs.
Peux tu maintenant écrire l'équation de cette réaction ?
Bonjour,
Oui je sais je ne m'en sors pas avec ça...
D'accord 
L'équation bilan s'écrit donc : H2NSO3H + HO- -> H2NSO3- + H2O
Est-ce juste? Si oui, je proposerais une équivalence
Merci
Bon jour
Je ne comprends pas de quelle manière je peux faire l'équivalence car il y a le même nombre de chaque coté. Ou n'est ce pas de cette manière qu'il faut s'y prendre?
Merci d'avance
L'énoncé (question 3) ne te demande pas de "faire l'équivalence"
On peut d'ailleurs se demander ce que signifie pour toi cette expression.
Il te demande une définition de l'équivalence.
C'est une question de cours.
Et il me semble bien que tu ne connais pas ce cours.
Il faut apprendre le cours avant d'essayer de faire les exercices qui s'y rapportent.
L'équivalence est le moment pour lequel les réactifs sont mélangés dans les proportions stoechiométriques.
J'ai le cours mais je ne le maitrise pas très bien et j'essaye de comprendre à l'aide d'exercices.
Par contre je n'ai aucune idée par rapport au tableau d'avancement de ce titrage pouvez-vous me mettre sur une piste svp?
Non l'équivalence n'est pas un "moment"
C'est un état du système pour lequel le réactif titrant et le réactif titré ont été introduits des des proportions stchiométriques.
Sais tu ce qu'est le réactif titrant ? Lequel est ce dans cet exercice ?
Mêmes questions pour le réactif titré.
Sais tu ce que sont les proportions stchiométriques ?
Quelles sont ces proportions dans cet exercice ?
Il est indispensable de savoir cela avant même de songer au tableau d'avancement.
d'accord merci.
Le réactif titré est l'espèce dont on veut déterminer la concentration (l'acide sulfamique) il est contenue dans la solution à doser (un détartrant pour cafetière) On utilise une solution titrante contenant un réactif titrant (soude) choisi en fonction de l'espèce à doser.
est-ce juste?
Les proportions stoechiométriques sont les proportions suivant lesquelles les produits se forment et les réactifs se combinent. Mais je ne parviens pas à les déterminer dans l'exercice...
Ta réponse est exacte en ce qui concerne le réactif titrant et le réactif titré.
Elle est correcte, mais incomplète, pour les proportions stchiométriques.
Ces proportions sont celles qui sont indiquées par les coefficients stchiométriques concernant les réactifs de l'équation de la réaction.
Cette équation étant ici ( voir question 2 ) :
(1) H2NSO3H +(1) HO- → (1) H2NSO3- + (1) H2O
les proportions stchiométriques sont ici de 1/1 donc autant de moles de H2NSO3H que de moles de HO-
On aura donc à l'équivalence la relation : n(H2NSO3H) = n(HO- )
Question 4 :
L'énoncé dit : "Compléter le tableau d'avancement de ce titrage. "
Le terme "compléter" indique qu'un tableau à compléter est présent dans l'énoncé.
Merci de poster ce tableau pour pouvoir t'aider à le remplir.
D'accord merci j'ai compris pour les proportions.
Le tableau d'avancement je n'ai pas réussi à l'insérer en photo du coup je l'ai recopié dans la conversation dans le message du 28/02/19 à 9'43.


