Inscription / Connexion Nouveau Sujet
Exercice de chimie
Bonjour,
j'aurai besoin de votre aide sur une question de mon long exercice ...
Une solution acqueuse de concentration molaire C = 5.0x10-1 mol.L-1, contient des ions cuivre II Cu2+(aq) et des ions chlorure Cl-(aq).
1. Ecrire l'équation de la réaction de dissolution dans l'eau du solide ionique qui a permis d'obtenir cette solution.
=> CuCl(s) -----> Cu2+(aq) + Cl-(aq)
2. Donner les valeurs des concentrations molaires effectives des deux ions en solutions.
=> [Cu2+(aq)] = [Cl-(aq)] = C = 5.0x10-1 mol.L-1
3. On verse dans un volume V = 100 mL de la solution précédente de la poudre de fer. Les ions cuivre II réagissent avec la poudre de fer, ce qui donne du métal cuivre et des ions fer II, Fe2+(aq). L'équation de la réaction associée à cette transformation est donnée dans le tableau d'avancement en annexe.
a. Calculer la quantité initiale n1 d'ions cuivre II.
=> avec les calcules que j'ai fais, je trouve n = 5.0x10-2 mol.L-1
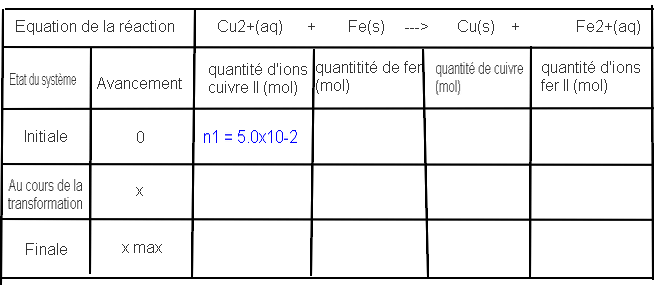
b. Compléter le tableau d'avancement en annexe, en utilisant des expressions littérales (n1 pour la quantité initiale d'ions cuivre II, n2 pour la quantité initiale de fer).
c. Sachant que le fer disparait complétement et que la quantité de cuivre formée est égale à 3.0x10-2 mol, calculer n2 en justifiant les résultats.
d. Calculer les concentrations molaires effectives des ions cuivre II et des ions fer II, à la fin de la transformation, en supposant le volume de la solution constant.
.
Je n'arrive donc pas à remplir le tableau demandé à la question b.
b. Compléter le tableau d'avancement en annexe, en utilisant des expressions littérales (n1 pour la quantité initiale d'ions cuivre II, n2 pour la quantité initiale de fer).
Il faut remplir par exemple, ligne 'Initial'
0 n1 n2 0 0
x x x x x
xmax x-xmax x-xmax x-xmax
x-n1 x-n2 pour savoir xmax