Inscription / Connexion Nouveau Sujet
Etude de la molécule PCl3
Bonjour!
J'ai un exercice à rendre au plus vite, mais j'ai beaucoup de difficultées à comprendre  ! POuvez-vous m'aider SVP
! POuvez-vous m'aider SVP 
Voici mon exercice et mes quelques réponces:
1) Rappeler les structures électroniques des atomes de chlore 17Cl et de phosphore 15P.
L'atome de chlore ; 17CL
Structure électronique = K2 L8 M7
L'atome de phosphore ; 5P
Structure électronique = K2 L8 M5
2) Soit la molécule PCl3. Combien d'électrons périphériques chaque atome apporte-t-il ? En déduire le nombre de doublets d'électrons de la molécule.
La molécule PCI3 est la structure électronique de l'atome de chlore 17CL, donc :
.La couche M n'a que 5 électron alors qu'elle peut en posséder 8 au maximum.
.Pour que l'atome soit noble, l'atome de phosphore veut avoir 8 électrons sur sa couche externe.
8-5=3
Le phosphore peut faire 3 liaison
Il y a3 chlore =>3 liaison dans PCl3 donc 3 doublets d'électrons
3)Combien d'électrons chaque atome doit-il engager dans des liaisons covalentes pour satisfaire la règle de l'octet ?
L'atome P doit donc gagner 3 électrons pour satisfaire la règle de l'octet.
4)Calculer le nombre total d'électrons appartenant aux doublets liants de PCl3. En déduire le nombre de doublets liants de la molécule.
( je ne sais absolument pas comment faire) 
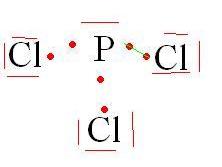
5)Connaissant le nombre total de doublets et le nombre de doublets liants, trouver la représentation de Lewis de la molécule.

6) Quel est l'atome central ? Que peut-on dire de la position des doublets électroniques qui l'entourent ?
L'atome centrale est l'atome de phostohore. Le reste j'ai des difficultés à répondre?? 
7)En déduire la forme de la molécule et dessiner sa représentation de Cram.
Schéma endessous, est-ce que c'est le bon?
Merci d'avance besoin d'une réponce au plus vite SVP MERCI 
Bonjour (et bonnes fêtes)
1) 2) et 3) ok très bien !
4) c'est la meme chose que pour la question 3) : il faut que tu détermines le nombre d'électrons engagés dans les liaisons covalentes pour les Cl !
Ok Merci pour la 1) la 2) et la 3) 
Pour la 4) je pense devoir répondre: 
6 électrons appartiennent au doublets liants de PCl3 ; 3 doublets liants appartiennent à la molécule.
c'est juste?
Pour la 5) je ne comprend pas 

Pour la 6)j'ai rajouter: L'atome centrale est l'atome de phostohore, les 4 atomes forments une pyramide.
Est-ce que pour la 7) le schéma est le bon?
Merci Encore ( ET BONNES FÊTES 
 )
)
Ok Merci pour la 1) la 2) et la 3)
Pour la 4) je pense devoir répondre:
6 électrons appartiennent au doublets liants de PCl3 ; 3 doublets liants appartiennent à la molécule.
c'est juste?
Pour la 5) je ne comprend pas
Pour la 6)j'ai rajouter: L'atome centrale est l'atome de phostohore, les 4 atomes forments une pyramide.
Est-ce que pour la 7) le schéma est le bon?
Merci Encore ( ET BONNES FÊTES )
Bonjour!
J'ai un exercice à rendre au plus vite, mais j'ai beaucoup de difficultées à comprendre  ! POuvez-vous m'aider SVP
! POuvez-vous m'aider SVP
Voici mon exercice et mes quelques réponces:
1) Rappeler les structures électroniques des atomes de chlore 17Cl et de phosphore 15P.
L'atome de chlore ; 17CL
Structure électronique = K2 L8 M7
L'atome de phosphore ; 5P
Structure électronique = K2 L8 M5
2) Soit la molécule PCl3. Combien d'électrons périphériques chaque atome apporte-t-il ? En déduire le nombre de doublets d'électrons de la molécule.
La molécule PCI3 est la structure électronique de l'atome de chlore 17CL, donc :
.La couche M n'a que 5 électron alors qu'elle peut en posséder 8 au maximum.
.Pour que l'atome soit noble, l'atome de phosphore veut avoir 8 électrons sur sa couche externe.
8-5=3
Le phosphore peut faire 3 liaison
Il y a3 chlore =>3 liaison dans PCl3 donc 3 doublets d'électrons
3)Combien d'électrons chaque atome doit-il engager dans des liaisons covalentes pour satisfaire la règle de l'octet ?
L'atome P doit donc gagner 3 électrons pour satisfaire la règle de l'octet.
4)Calculer le nombre total d'électrons appartenant aux doublets liants de PCl3. En déduire le nombre de doublets liants de la molécule.
je pense devoir répondre  :6 électrons appartiennent au doublets liants de PCl3 ; 3 doublets liants appartiennent à la molécule.
:6 électrons appartiennent au doublets liants de PCl3 ; 3 doublets liants appartiennent à la molécule.
5)Connaissant le nombre total de doublets et le nombre de doublets liants, trouver la représentation de Lewis de la molécule.
Je n'y arrive pas 
6) Quel est l'atome central ? Que peut-on dire de la position des doublets électroniques qui l'entourent ?
L'atome centrale est l'atome de phostohore, les 4 atomes forments une pyramide.
7)En déduire la forme de la molécule et dessiner sa représentation de Cram.
Schéma si-dessous, est-ce que c'est le bon?
Pouvez-vous me dire si les réponces que j'ai répondu sont justes et m'aider pour celle ou j'ai des difficultées SVP
Merci d'avance besoin d'une réponce au plus vite SVP MERCI
** image effacée **
*** message déplacé ***
Edit Coll
5) tu l'as dessiné à la question 7...
6) ok
7) dans une représentation de Cram il faut qu'il y ait une liaison dans le plan, une liaison vers l'avant et une liaison vers l'arrière...(c'est une représentation en perspective)
LOl par contre la 7 je galere autant ...
"dans une représentation de Cram il faut qu'il y ait une liaison dans le plan, une liaison vers l'avant et une liaison vers l'arrière...(c'est une représentation en perspective)"
Tu saurais m'en dire plus ^^ ?
Merci.
Oui par exemple la molécule de NH3 est représentée comme ceci :
(trait simple : liaison dans le plan, trait triangulaire : liaison vers l'avant et trait pointillé : liaison vers l'arrière)
OK?


