Inscription / Connexion Nouveau Sujet
Esters
Bonjour à tous,
Voilà j'ai un exercice sur les esters et je voulais savoir si mes réponses sont justes.
Voici l'énoncé:
On fait un chauffage à reflux de 0,40 mol d'acide méthanoïque et 0,40 mol de propan-2-ol. On ajoute quelques gouttes d'acide sulfurique. Au bout d'une heure, on détermine par titrage la quantité de matière restante d'acide méthanoïque, soit n = 0,18.
1) Quel ester obtient-on ? Le nommer.
Bon alors ici j'ai fait:
O O
// //
HC + CH3-CH-CH3 = H2O + HC
\ | \
OH OH O-CH2-CH2-CH3
On obtient donc du méthanoate de propyle (ici je ne suis pas du tout sûre).
2) Tableau d'évolution de la réaction.
Bon ici, j'ai regardé plusieurs exercices et les produits étaient déjà présents dans l'état initial, mais ici je ne vois pas pourquoi je devrais les mettre.
n(acide méthanoïque) n(propan-2-ol) n(ester) n(eau)
ni = 0,40 mol ni = 0,40 mol 0 0
nint = 0,40-x mol nint = 0,40-x x x
nf = 0,18 mol nf = 0,40-xf xf xf
Voilà ici également mon tableau me semble étrange...
3)a. Quel est la valeur de xeq ?
Bon là j'ai fait d'après le tableau, 0,40-xeq = 0,18 donc:
xeq = 0,40-0,18 = 0,22 mol
b. Exprimer K en fonction de xeq et la calculer.
K = [ester]eq²/[acide méth.]eq²
= xeq²/(0,40-xeq)²
= (0,22)²/(0,18)²
= 1,5
4) Calculer le rendement de cette estérification.
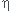 = n(ester)/nt (nt = quantité de matière si la réaction était totale)
= n(ester)/nt (nt = quantité de matière si la réaction était totale)
= xf/ni(ac.méth.) (car si nt=xmax, alors xmax=ni(reactif limitant)
= 0,22/0,40
= 55%
Je ne suis vraiment pas sûre de mes réponses.. Pourriez-vous me dire si mes réponses sont justes ?
En vous remerciant 
Oh mon schéma est mal resté !
En fait l'oxygène avec la double liaison et la chaine O-CH2-CH2-CH3 sont reliés au dernier HC 
Bonjour,
1. OK
2. OK
3.a. OK
3.b. Attention, on n'est pas en solution aqueuse donc on ne peut pas définition de concentration. Il faut donc considérer les quantités de matière (en fait, seule ta première ligne de "définition" est fausse, les calculs sont justes par la suite ; mais pourquoi écris-tu x_f à des endroits et x_éq à d'autres ? choisis une seule notation pour tout l'exercice)
4. OK
Bilan : c'est très bien dans l'ensemble 
P.S. : L'exercice a choisi la notation x_éq donc remplace les x_f de ton tableau d'avancement par x_éq.
Oui en fait xeq = xf, j'ai un peu mélangé les deux..
Par contre pour la 3)b. comme on n'a pas de volume donné, j'en ai déduit que pour V = 1L, on a C = xeq
Merci d'avoir pris le temps de regarder mes réponses 
A bientôt.
Par contre pour la 3)b. comme on n'a pas de volume donné, j'en ai déduit que pour V = 1L, on a C = xeq
Non ! Comme je l'ai dit plus haut, on n'est pas en solution aqueuse : on ne peut donc pas définir de concentration !
Vous avez dû écrire dans le cours, que
Voilà, voilà

Ah d'accord ! Peut être que nous l'avons écrit dans le cours, je dois avouer que je ne l'ai pas regardé avant de faire l'exercice 
Merci encore ! 
Cette histoire de "concentration" est assez délicate et on ne rentre pas dans les détails en terminale. Peut-être que ton professeur vous a dit deux mots sur l'activité d'une espèce ? C'est avec cette notion qu'on définit la constante d'équilibre. Tu comprendras ça l'année prochaine si tu connais à faire un peu de chimie 
Euh non notre professeur ne nous a pas parlé d'activité d'une espèce.. Comme vous le dites, je verrai ça l'année prochaine, en effet 
Très bien oublie ma remarque alors !
Par contre, il faut que tu retiennes que la constante d'équilibre se définit à l'aide des concentrations en solution aqueuse (comme lorsque vous avez parlez des couples acide/base, du pH, etc.) et à l'aide des quantités de matière sinon (comme pour l'estérification où on n'est pas en solution aqueuse : l'eau n'est pas le solvant mais un produit de la réaction).
Bon après-midi ! 


