Inscription / Connexion Nouveau Sujet
éspèces chimiques inflammables
Bonjour, pourriez vous m'aider à faire cet exercice de chimie?
a) dans certains laboratoires, on trouve sur certains flacons l'étiquette ci-contre. Que signifie ce pictogramme, et quellees précautions faut-il prendre lors de la manipulationd e tels flacons?
b)La combustion d'une éspèce chimique esy une réaction mettant en jeu le dioxygène de l'air. Ecrire l'équation de combustion de l'éther, éspèce chimique de formule C4H10O, sachant que les seuls produits de la combustion sont le dioxyde de carbone et l'eau.
c)Un flacon contient un volume VE = 1,00L d'éther. Quelle est la quantité de matière nE d'éther dans un tel flacon sachant que la masse volumique de cette éspèce chimique est  E = 0,796g.cm-3?
E = 0,796g.cm-3?
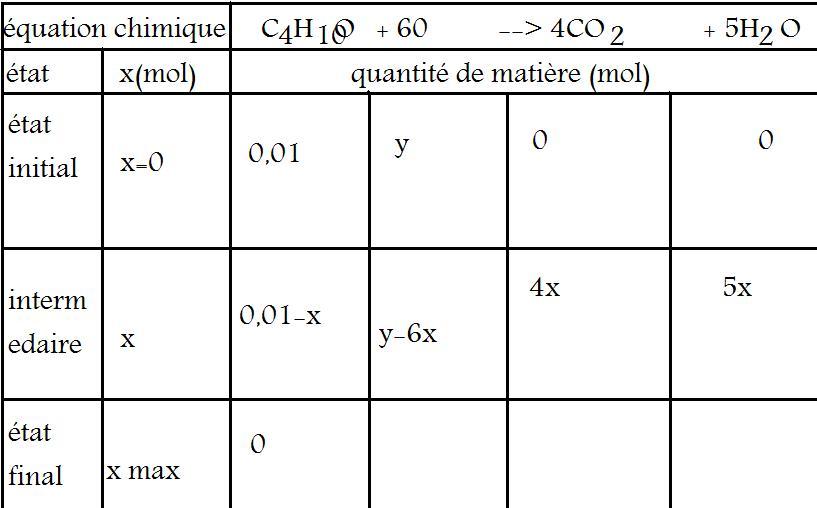
d)A l'aide d'un tableau d'avancement, déterminer la quantité de matière de dioxygène necessaire pour bruler la totalité du litre d'éther.
e)Déterminer également les quantités de matière de dioxyde de carbone et d'eau produites par la combustion de tout l'éther.
début de réponses:
a)Ce pictogramme siginfie que la solution dans le flacon est inflammable, il ne faut donc pas la laisser près d'une flamme ou à la chaleur.
b)C4H10O + O2 CO2+ H2O
CO2+ H2O
faut il l'équilibrer?
c)M(C4H10O ) = 74,0 g.mol-1
je ne suis pas sure de la façon de faire la suite..
merci d'avance

Bonjour,
a. TB !
b; A équilibrer :
...C4 H10 O +...O2 ---> ...CO2 + ...H2O
c. Utilise p = m/V <=> me = pe.Ve puis ne=me/Me.
d. Tableau à faire.
e. Utiliser le tableau.
b) je vais équilibrer
c) c'est ce que j'ai commencé à faire
d) et e) tu pourras un peu m'aider?
merci beaucoup beaucoup
c)
M(C4H10O) = 16,0 X 1 + 1,0 X 10 + 12,0 X 4 = 74,0 g.mol-1
m(C4H10O)=  (C4H10O)X V(C4H10O)
(C4H10O)X V(C4H10O)
m(C4H10O)= 0,796 X 1
m(C4H10O)= 0,796 g
n(C4H10O)= m(C4H10O)/ M(C4H10O)
n(C4H10O)= 0,796/74,0 = 0,01 mol
est ce juste?
A l'état maximal,
0,01 - xmax = 0 donc xmax = 0,01 mol car tout l'éther est consommé.
Donc y - 6xmax = 0 <=> y = 6xmax = 0,06 mol