Inscription / Connexion Nouveau Sujet
enthalpie enthropie
Voila cet exercice me pose particulièrement problème, je ne comprend pas la technique qu'il faut suivre pour trouver le résultat:
Soit la réaction suivante qui sera ensuite dénommée réaction 1
CN2H40(s) + (3/2)O2(g)  N2(g) + CO2(g) + H20(l)
N2(g) + CO2(g) + H20(l)
on donne a 298 K:
∆fH°(CO2(g))= -393,1 Kj.mol^-1
∆fH°(H20(l))= -285,6 Kj.mol^-1
∆fH°(CN2H40(s))= -326,4 Kj.mol^-1
S°(C02(g))= 213,6 J.mol^-1.K^-1
S°(H20(l))= 69,8 j.mol^-1.K^-1
S°(O2(g))=204,8 J.mol^-1.K^-1
S°(N2(g))= 191,4 J.mol^-1.K^-1
On recherche l'enthalpie standard de la réaction 1 à 198K
On dois trouver qu'elle est comprise entre -637 Kj.mol^-1 et -639 Kj.mol^-1
Je connais les formules du cours tels que ∆rH°=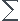 vi∆fH°i avec vi>0 pour les produit et vi<0 pour les réactifs et quelques autres encore mais je ne sais pas comment les mettre en relation pour trouver le ∆fH°(N2(g)) ici manquant.
vi∆fH°i avec vi>0 pour les produit et vi<0 pour les réactifs et quelques autres encore mais je ne sais pas comment les mettre en relation pour trouver le ∆fH°(N2(g)) ici manquant.
Ce genre d'exercice me pose beaucoup de problème si vous pouvez m'éclairer sur les étapes à suivre ça serait un bonheur. Merci!
- les deltafH° des corps simples sont nulles donc deltafH° de O2 et N2 = 0
- tu vas , par la formules que tu indiques calculer deltarH° de la réaction 1 à 298K
- pour calculer deltarH° à une autre température il faut utiliser la loi de Kirchhof et pour cela il faut que tu connaisses les Cp des différents composés qui interviennent dans cette réaction
@ anniejeanne
Je ne sais pas quoi dire... Comme mon cours ne montre que quelques exemples d'éléments a leurs états standard de référence, et que le N2 n'y apparaissant pas, je ne l'ai pas pris en compte.
Je sais maintenant que cela s'applique a tout les éléments dans leurs état de référence !
merci de ta réponse.
Cependant maintenant que je continu la suite de l'exercice, il m'advient un autre soucis pour la suite de l'exercice:
trouver l'entropie molaire standard de CN2H40(s)
je sais que le calcul se fait de la façon suivante : 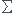 ∆rS°=vi∆rS°i
∆rS°=vi∆rS°i
mais il nous manque 2 données, ∆rS° et S°(CN2H40(s))
de plus par la suite l'exercice nous demande de calculé le ∆rG° qui se calcul facilement de la façon suivante : ∆rG°=∆rH°-T∆rS° mais sans T∆rS° impossible de continué jusque là...
- pour t'en sortir avec les entropies il te manque une donnée : soit deltarS° et tu en déduiras S° de CN2H4O soit on te donne S° de ce composé et tu en déduiras deltarS° ...
- effectivement tu pourras ensuite calculer deltarG°
donc , avec les données indiquées : exo impossible !


