Inscription / Connexion Nouveau Sujet
Dosage spectrophotométrique de la vanilline.
Bonjour j'aimerai avoir de l'aide pour un devoir maison sur lequel je bloque.
Voici l'énoncé :
Le spectre d'absorption de la vanilline, pour une longueur d'onde comprise entre 200 et 800nm ne présente qu'une unique absorption de 348nm.
a) La vanilline est elle colorée ? Justifier.
b) Quelle loi, reliant l'absorbance à la concentration, permet de tracer une courbe d'étalonnage reliant linéairement l'absorbance d'une solution à sa concentration en vanilline ?
c) Pourquoi choisir de mesurer l'absorbance de la solution pour une longueur d'onde de 348nm ?
Droite d'étalonnage : Dans une fiole jaugée de V0=1,000L, préparer une solution mère F0 contenant m=100mg(soit 0,6579mmol) de vanilline et 4g d'hydroxyde de sodium. Préparez par ailleurs un litre d'une solution S0 d'hydroxyde de sodium (CH0-=0,1mol.L, soit 4 g d'hydroxyde de sodium par litre d'eau). Dans une fiole jaugée de volume V1=100ml, introduire à la pipette jaugée V2=1,00 ml de F0 et ajouter S0 jusqu'au trait de jauge, F1 est cette solution fille. Préparez de même les solutions F2 à F6 en diluant, dans des fioles de 100ml, les volumes V=2;3;4;5;6ml de F0 avec S0. Mesurez l'absorbance A de ces différentes solution à 348nm et tracer la droite A=f(c).
d) A l'aide du document "Droite d'étalonnage" , déterminer la concentration molaire c1 en vanilline de la solution F1 sachant que la masse molaire de la vanilline est M=152.2 g/mol
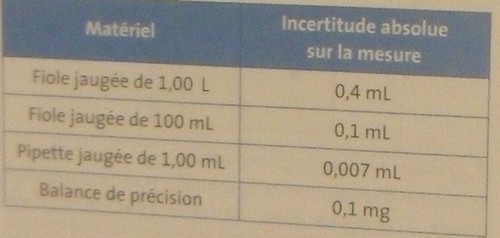
Les incertitude relative sur c1 est la somme des incertitudes relative sur m,V0,V1 et V2.
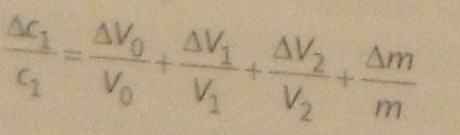
e) En comparant les incertitudes relatives, préciser quelle est la principale source d'incertitude sur la concentration de la solution F1.
f) Déterminez avec son incertitude la valeur de c1.
g) A partir des résultats expérimentaux réunis dans le tableau ci-dessous, tracer la droite étalonnage de l'absorbance en fonction de la concentration c en vanilline.

h) Déduire du spectre d'absorption de la solution de sucre vanillé (voir ci dessous) la quantité de matière ainsi que la masse de vanilline dans un sachet de 7.5 grammes.
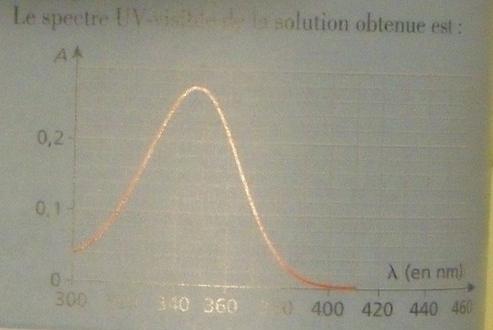
Voilà pour le moment j'ai fait cela :
a) Elle n'est pas colorée elle n'est pas situé dans le domaine du visible.
b) Loi de Beer-Lambert A = k * c
c) Unique pic d'absorbance donc impossible de faire une mesure ailleurs.
d) ?
e) La masse est la principale source d'incertitude.
f) Impossible sans c1.
g) ?
C'est surtout la question d qui me bloque. En espérant avoir de l'aide de votre départ sans me donner les réponses mais me mener sur le bon chemin.
Merci.
Salut  !
!
a) Oui, agrémente simplement des valeurs
b) très bien
c) oui très bien
d)
Dans une fiole jaugée de volume V1=100ml, introduire à la pipette jaugée V2=1,00 ml de F0 et ajouter S0 jusqu'au trait de jauge, F1 est cette solution fille.
assez maladroite l'introduction de V2, ils auraient pu faire attention -_-'
Principe de la dilution : la quantité de matière ne varie pas donc n0 = n1
ce qui mène à C0*V0 = C1*V1
Mais ici avec la maladresse de l'énoncé tu dois transcrire par :
C0*V2 = C1*V1
Pour déterminer C0 tu considères m (attention à convertir en g), M et un volume de 1 L qui est V0
e) oui
g) Trace juste un graphique
Merci de ta réponse, mais qu'entends tu par "Pour déterminer C0 tu considères m (attention à convertir en g), M et un volume de 1 L qui est V0" ?
Oui voici le détail de mes calculs :
Pour déterminer C0 je fais :
m/M = 0.1 /152.2 = 6.57 e-4
C 0= n/V0 = 6.57 e-4 / 1 = 6.57 e-4
D'où
C0 * V2 = C1 * V1
6.57 e-4 x 0.001 = C1 * 0.1
6.57 e-7 = C1 * 0.1
6.57 e-7 / 0.1 = C1
Et donc je trouve 6.57 e -7 pour C1 sachant qu'après j'ai un tableau avec F2 F3 etc, avec des concentrations en puissance -5 donc je trouve ca bizarre..
On te donne déjà la concentration dans l'énoncé :
m=100mg(soit 0,6579mmol)
Au temps pour moi, c'est ce que j'ai sur ma feuille de brouillon mais j'ai mal retranscrit d'où la confusion

Et bien j'avais normalement trouvé la masse comme, étant avec le plus d'inceritude mais en refaisant mes calculs je trouve la même chose pour V1 et la masse soit 1e-3


