Inscription / Connexion Nouveau Sujet
dm sur les dosages
Voici l'énoncé;
"Etude d'un dosage du dioxyde de soufre présentanun vin.
le dioxyde de soufre (gaz de formule SO2) est soluble dans l'eau.
En solution aqueuse, c'est le reducteur SO42-(aq)/ SO2.
Pour éviter une oxydation du vin, on y ajoute a un moment de sa fabrication du dioxyde de soufre; toutefois,sa concentration est legalement limitée.
Afin de verifier la conformité de cette concentration, on realise le dosage suivant:
Dans un bêcher, on verse un volue V=25mL de vin blanc. On y ajoute un peu d'acide sulfurique afin d'acidifier le milieu.
On utilise une solution titrante de diiode (I2) de concentration [I2]= 7.80.10-3.mol.L-1 que l'on ajoute lentement dans le bêcher contenant le prélévement cité précédemmet tout en y agitant."
voici les questions que je n'arrive pas a traiter:
- Etablir, en le justifiant le bilan de la transformation chimique utilisée ici comme "outil" du dosage.
Rq: I2 est l'oxydant du couple I2/I-(aq)
justifier la necessité de l'acidité du milieu.
- Sachant que le volume de la solution I2 necessaire à l'obtention de l'équivalence est Veq= 6.10 mL, determiner à l'aide d'un tableau d'avancement la concentration en SO2 de l'échantillon de vin blanc testé.
- Sachant que la concentration massique maximale permise légalement en dioxyde desoufre est 210mg.L-1, ce vin est il confonrme a la légalité? (justifiez vos calculs)
donneés: M(O)= 16g.mol-1 M(S)=32.1g.mol-1
- Sachant que la mase molaire atomique de l'iode est M(I)= 126.9 g.mol-1, proposer une méthode compléte de préparation de la solution titrante de diiode qui a servi a ce dosage.
Voila c'est une partie de mon DM de chimie que j'ai a faire pendant les vacances mais je n'arrive pas a traiter ces question donc une aide serait la bien venue! merci d'avance a toutes celles ou tout ceux qui m'aiderons! 
Salut!
- Etablir, en le justifiant le bilan de la transformation chimique utilisée ici comme "outil" du dosage.
Rq: I2 est l'oxydant du couple I2/I-(aq)
justifier la necessité de l'acidité du milieu.
Ecris les demi-équations au préalable...
Pour l'acidité je te l'ai expliqué dans l'autre topic

- Sachant que le volume de la solution I2 necessaire à l'obtention de l'équivalence est Veq= 6.10 mL, determiner à l'aide d'un tableau d'avancement la concentration en SO2 de l'échantillon de vin blanc testé.
Tu établis ton tableau d'avancement à partir de l'équation de la réaction. Pour calculer les quantités de matière tu utilises C.V...
- Sachant que la concentration massique maximale permise légalement en dioxyde desoufre est 210mg.L-1, ce vin est il confonrme a la légalité? (justifiez vos calculs)
donneés: M(O)= 16g.mol-1 M(S)=32.1g.mol-1
Tu fais à partir des résusltats du tableau d'avacement. Tu utilises la formule Cm = c.M
- Sachant que la masse molaire atomique de l'iode est M(I)= 126.9 g.mol-1, proposer une méthode compléte de préparation de la solution titrante de diiode qui a servi a ce dosage.
Tu décris le protocole d'une dissolution... Tu pèses le diiode avec la balance (tu as calculé m = n*M). Tu l'introduis dans la fiole jaugée avec entonnoir, rince en prenant garde que l'eau de rinçage finisse dans la fiole. Tu remplis aux 2/3 avec de l'eau distillée, bouche puis agite. Tu complètes jusqu'au trait de jauge en terminant avec un compte-gouttes, bouge et homogénéise...
Ok?
Je te rép ce soir après le repas j'ai un rdv ce soir

Je suis en train de faire le tableau d'avancement mais j'arrive pas a calculer pour S02 comment on fait. j'ai l'impression qu'il n'y a pas assez de données.
parce que pour pouvoir fait C.V il faut avoir le volume et la concentration, or on a que le volume (25 mL) mais pas la concentration...
jvoit pas comment calculer pour SO2!! j'ai fait le tableau d'avancement mais j'ai pu remplir que la partie sur I2! aidez moi svp!!
je voudrais juste une aide, une indication ...
merci
Salut!
Désolé du retard, j'étais d'anniversaire
Tu cherches la concentration donc c'est normal que tu ne l'ais pas.
Je t'ai dit d'utiliser le volume équivalent...
A l'équivalence n = n'
donc C.V = C'.V'.
Tu appliques la même relation avec Véq
Non le volume équivalent correspond au volume de diiode versé...
Tu as C.V = 7,80.10-3*6,0.10-3.
O tu doses 25 mL.
Donc V = 25 mL.
Et tu as la relation: C = (C'.Véq)/V
donc C = (7,80.10-3*6,0.10-3)/(25.10-3).
Ok?
si j'ai bien compris on a alors dans la première ligne du tableau d'avancement :
pour I2 : n= C. Veq = 7.80* 10-3 * 6.10*10-3 = 4.76* 10-5
pour S02:
C = (C'.Véq)/V
j'ai commencé le tableau d'avancement le voici. il n'est absolument pas du tout complet mais j'estime que c'est un commencement

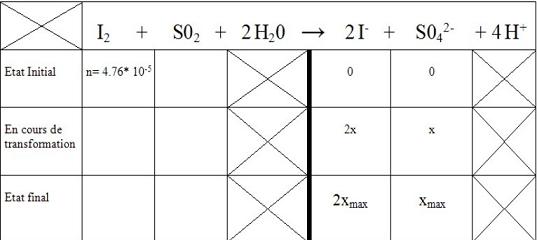
UN très bon début même
à l'aide d'un tableau d'avancement la concentration en SO2 de l'échantillon
Si tu veux la quantité de matière il te faut trouver C...
Enfin je t'ai donné cette méthode qui s'applique sans tableau d'avancement, donc il te faut utiliser n = C'.V', donc ce que tu as dit...
oui! ce que j'ai dit n'avais pas vraiment de sens ...
donc
C = (C'.Véq)/V
C= (7.80*10-3*6.10.10-3) / 25.10-3
C = 4.758.10-5/25.10-3
C= 1.9032.10-3 mol/L
c'est exact?
C = (C'.Véq)/V
C= (7.80*10-3*6.10.10-3) / 25.10-3
C = 4.758.10-5/25.10-3
C= 1.9032.10-3 mol/L
Donc n= C.V
n = 1.9032.10-3 * 25.10-3
n= 4.758.10-5 mol
n≈ 4.76.10-5 mol
donc voici le tableau d'avancement complété mais je ne sais pas s'il est correct...
pour l'état final et en cours du dosage comment fait-on pour x et xmax?
Tu remplaces x par xmax puis tu calcules
4,76.10-5 - xmax = 0 donc xmax = 4,76.10-5 mol.
A toi de finir
Donc voila la fin, j'espére qu'elle est bonne ... :-S
sinn pour la question d'aprés:
- Sachant que la concentration massique maximale permise légalement en dioxyde desoufre est 210mg.L-1, ce vin est il confonrme a la légalité? (justifiez vos calculs)
donneés: M(O)= 16g.mol-1 M(S)=32.1g.mol-1
tu procéderé comment?

MSO4= M(S) + 4 M0
MSO4= 32.1+ 4*16
MSO4= 96.1 g /mol
donc Cm=1.9032*10-3 * 96.1
Cm= 0.1828.. donc ce vin n'est pas conforme a la légalité
0.182 g.L-1
par contre je ne comprend pas pourquoi tu dit que c'est un seuil maximal, il est tout de même conforme non?
Sachant que la concentration massique maximale permise légalement en dioxyde desoufre est 210mg.L-1, ce vin est il confonrme a la légalité
C'est 210.10-3 g.L-1 soit 0,210 g.L-1.
Or tu es à 0,182 g.L-1 cad 182 mg.L-1 donc conforme à la législation...
Attention aux unités...
a oui!
pour la dernière question je trouverai toute seule ^^
je te remercie beaucoup de m'avoir aidé!
a bientot jsp 
Oki si tu veux la faire corriger je reste à ta disposition, et pas de quoi
Bonne fin de journée et bonne continuation
Adiù



