Inscription / Connexion Nouveau Sujet
Dm atomes naturels
1) Combien d'éléments chimiques possèdent au moins un atome naturel ?
2) Sachant que l'on connaît actuellement 118 éléments chimiques, combien d'éléments chimiques ne possèdent aucun atome naturel ?
3) Calculer la masse en grammes d'un échantillon naturel de 6.0x10^23 atomes de chlore (Z=17)
Donnée pour le calcul:masse protons: 1.67x10^-27kg
kg= 1.67x10^-24g
Il n'y a pas d'énoncé, c'est juste ces questions. En ce qui concerne mes propositions, j'ai cherché mais c'est sans grand succès.
bonjour,
la règle sur le forum est de taper l'énoncé.
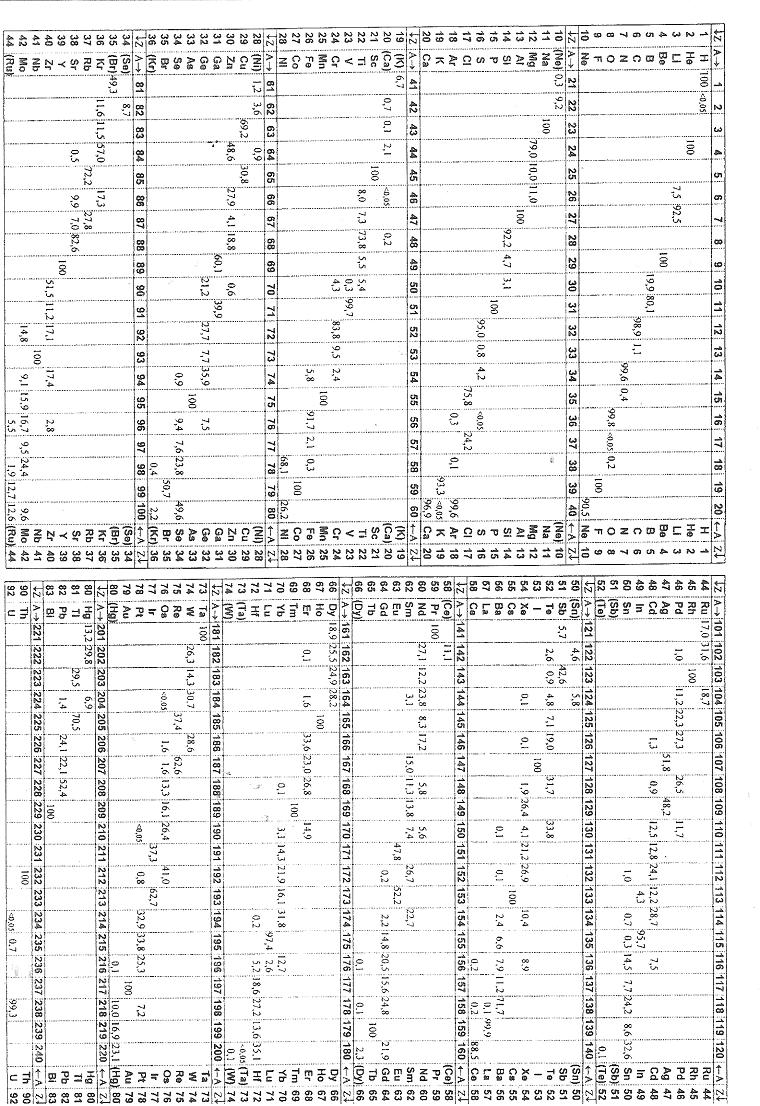
indique aussi les questions pour lesquelles tu as trouvé la réponse (la plupart des réponses se trouvent dans les tableaux)
certes mais je ne pouvais pas recopier le tableau c'était juste en aide à hamza94 qui à posté le message 
ok  je pensais que tu voulais de l'aide pour répondre aux questions, en fait seul le tableau était utile
je pensais que tu voulais de l'aide pour répondre aux questions, en fait seul le tableau était utile
excuse-moi !
3) calcul d'abord la masse d'un atome de chlore sachant que la masse d'un atome est très voisine de la masse de l'ensemble de ses protons
bonjour,
j'ai le même Dm à traiter pour demain je suis vos explications donc si j'ai bien compris je fais :
17x1.67*10^-24
puis le résultat multiplié par 6.0.10^23 ?
ai-je bon ?
1)L'adjectif naturel signifie que l'élément est présent dans la nature
2)isotopes du carbones : C12 et C13
3) pas d'isotopes naturel car atome artificiel
4) ?
5)?
6) il y a 92 atomes naturels
pour la masse c'est juste
4) il faut compter tous les éléments du tableau (certains entre parenthèses apparaissent 2 fois)
6) il faut compter tous les atomes du tableau isotopes compris
Nebelwerfer
pour la 7) il faudrait en effet placer les 92 éléments donc beaucoup plus d'atomes mais en en plaçant seulement quelques uns tu devrais voir apparraître le droite.
l'hydrogène est un élément mais il y a différentes formes:
- l'ion hydrogène
- les isotopes de l'atome d'hydrogène
L'élément c'est ce qui permet de définir un "objet" chimique qui peut avoir plus compositions mais qui a un numéro atomique bien précis.
Un atome correspond à une des compositions de l'élément, en plus d'avoir un numéro atomique précis (c'est à dire son nombre de protons) il a un nombre de neutrons et d'électrons déterminé
ok merci beaucoup il y a juste encore pour le graph ou je "galère " un peu je pense que je n 'ai pas tous saisi.
exemple du carbone Z=6, deux isotopes naturels A=12 et A=13
il faut donc placer 2 points sur le graphe :
- (6;6)
- (6;7)
et procéder comme cela pour tous les atomes naturels (bon courage!!!)