Inscription / Connexion Nouveau Sujet
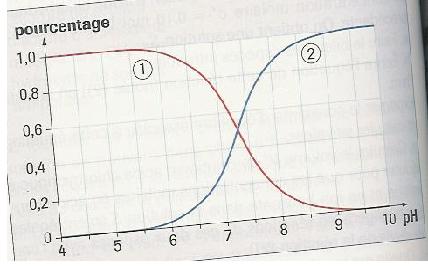
Diagramme de distribution
D'aprés la courbe j'ai trouvé que le pka = Ph = 7.3 car [ClO-]eq=[ClOH]eq . Ensuite on nous dit qu'on mélange un certain volume d'acide hypochloreux avec une solution d'hydroxyde et le pH de la solution obtenue vaut 7.3 . De plus ,on nous demande de calculer le rapport [ClO-]eq/[ClOH]eq de la solution obtenue .
Ma question est la suivante : Le pka change-t-il lorsque l'on rajoute la solution d'hydroxyde?? Car lorsque je calcule le rapport en utilisant la relation pH=pKa + log([base]/[acide]) je trouve 1 et cela ne me semble pas trés juste .
Merci d'avance pour vos réponses 
Bonjour,
Non, le pKa ne varie pas, sauf avec le température, tout comme le Ka, car il caractérise l'équilibre d'une réaction.
merci pour vos réponses c'est plus clair comme ça  ; mais j'ai encore un autre problème car ensuite on nous demande de faire un tableau d'évolution et de déterminer l'avancement final à partir du rapport calculé . J'en ai déduit que [ClO-]eq=[ClOH]eq donc d'aprés le tableau d'avancement on a que la quantité de matière de ClO- (c'est-à-dire xF) est égale à la quantité de matière de ClOH . J'ai trouvé xF=2.0*10^-4 . Ensuite on nous a demandé de calculer le taux d'avancement final , j'ai calculé xmax et là je trouve xmax = n(OH-)=1.0*10^-4 donc taux d'avancement final = Xf/Xmax = 2 (ce qui me semble complètement faux).Je ne trouve pas mon erreur .
; mais j'ai encore un autre problème car ensuite on nous demande de faire un tableau d'évolution et de déterminer l'avancement final à partir du rapport calculé . J'en ai déduit que [ClO-]eq=[ClOH]eq donc d'aprés le tableau d'avancement on a que la quantité de matière de ClO- (c'est-à-dire xF) est égale à la quantité de matière de ClOH . J'ai trouvé xF=2.0*10^-4 . Ensuite on nous a demandé de calculer le taux d'avancement final , j'ai calculé xmax et là je trouve xmax = n(OH-)=1.0*10^-4 donc taux d'avancement final = Xf/Xmax = 2 (ce qui me semble complètement faux).Je ne trouve pas mon erreur .
données:"on mélange un volume V1=20 mL d'acdide hypochloreux de concentration enn soluté apporté c=1.0*10^-2 mol.L^-1 avec un volume V2=10 mL d'une solution d'hydroxyde de sodium de concentration en soluté apporté c=1.0*10^-2 mol.L^-1 . Le pH de la solution obtenue vaut 7.3 .


