Inscription / Connexion Nouveau Sujet
Déterminer la formule d'une amine saturée
Bonjour, j'aurais besoin d'un petit coup de main sur l'exercice suivant (Chimie 1S)
On cherche à déterminer la formule d'un amine saturée. Pour celà, on réalise le dosage d'une solution aqueusee de cette amine, obtenue en mettant en solution m=1,0 g de cette amine dans un volume d'eau valant approximativement 30mL. Il faut verser, à l'aide de la burette, un volume V1=33,9mL d'acide chlorydrique de concentration C1=0.50mol.L-1 pour atteindre l'équivalence.
1- Ecrire l'équation de la réaction servant de support à ce dosage.
2- Déterminer la quantité de matière d'amine ainsi dosée.
3- En déduire la masse molaire moléculaire de cette amine.
4- Déterminer alors la formule brute de cette amine
5- Donner les formules semi-développées et les noms des molécules R-NH2 (amine primaire) dont la formule brute à été établie plus haut.
Voici ce que j'ai fais :
1- amine + HCl = R-NH2
2- Je ne suis pas sûre de ma réponse à la premère question, et même avec delle cie, je ne vois pas trop comment y arriver. Je sais que n=m/M Il faudrait donc calculer la masse molaire de l'acide chlorydrique
3- Je ne peux pas répondre aux questions suivantes car elles dépendent les unes des autres.
Merci pour votre aide 
Bonjour
1) non non. L'amine (quelle soit primaire, secondaire ou tertiaire) va attaqué l'H+ pour donner un cation selon la réaction :
R1, R2 et R3 peuvent etre soit des H soit des groupes alkyles (CH3, CH3-CH2-, ...)
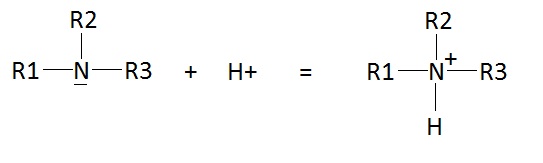
2- Les coefficient steochiométriques sont respectés ?
Je ne comprends pas la notation pour la réponse à la 1, pourquoi N+ ? Comment arrives t'on à cette réponse ? Doonc l'amine réagit avec l'eau mais pas avec HCL ?
1) heu non l'amine ne réagit pas avec l'eau (je peux me tromper...)
Le doublet non liant de l'amine réagit avec le H+ pour fromer une liaison.
1) oui pardon je n'ai pas préciser comme si c'était évident... effectivement l'amine réagit avec l'H+ provenant de l'acide chlorhydrique (combinaison de H+ et de Cl-)
ok?
Pour le 1 c'est ok, merci beaucoup. Maintenant, pour le 2, il faut respecter les coefficients stoechiométriques ? n=m/M , mais comment avoir M de l'amine ?
C=n/v
donc n=C*V
donc n(HCL)=0.50*33,9=16,95. Les proportions stoechiométriques sont égales à 1, donc n(HCL)= N(amine)= 16.95mol
attention le volume équivalent est égal à 33,9 mL (et non pas 33,9 L)
ca donne donc namine=16,95*10-3 mol
3) Mamine=59 g/mol tu es d'accord?
oops...
oui, je comprends, maintenant qu'on à n, on fait n=m/M donc M=n*m.
La formule brute est sous la forme Cn H2+2 ? Comment la trouver ?
3) Attends tu as marqué : M=n*m non c'est faux !! attention !! m=n*M donc M=?
4) la formule brute d'une amine est : CnH2n+3N
M=n/m
 Je te rappelle que la formule est m=n*M !!!
Je te rappelle que la formule est m=n*M !!!
comme n c'est 16.95, la formule c'est C17H37N ?
Donc la formule brute d'une amine est CxH2x+3N (excuse moi pour la notation qui prête a confusion)
Merci beaucoup pour votre aide, mon exercice à été corrigé aujourd'hui, vous m'avez mise sur la voie. A noter que la formule d'une amine saturée est CnH2n-1N. =)
Encore merci beaucoup 
A noter que la formule d'une amine saturée est CnH2n-1N. =)
c'est faux
si on prend l'exemple simple CH3NH2 ou CH5N,
on a bien CnH2n+3N
C'est la correction que j'ai eu par mon prof de physique il y à peine 5heures ! J'irais redemander, mais je prends bien mes corrections.
Je me suis effectivement trompée hier dans mon affirmation sur l'amine. Je vous donne la correction qui a été faite en cours vendredi. Merci à vous.
1
H3O+ = H++H2O
R-NH2+H+ = R + N+H3
__________________________________
H3O+ + R-NH2--> R-N+H3 + H2O
Le schéma de lulu3436 nous a été donné à titre indicatif.
2
A l'équivalence
n(amine)/1=n(acide)/1=C1*Ve = 0.50*33.9.10-3=17.10-2
Ce qui correspond à ce qui a été dit.
3
M=12n+2n+1+16=59
4 n=(59-17)/14=3 d'où C3H9N car la formule générale d'une amine saturée est CnH2n+1-NH2 --> ce qui en réalité peut aussi s'écrire comme vous l'avez fait, excusez moi de vous avoir contre dit.
5 Ch3-Ch2-Ch2-NH2
Propanamine


