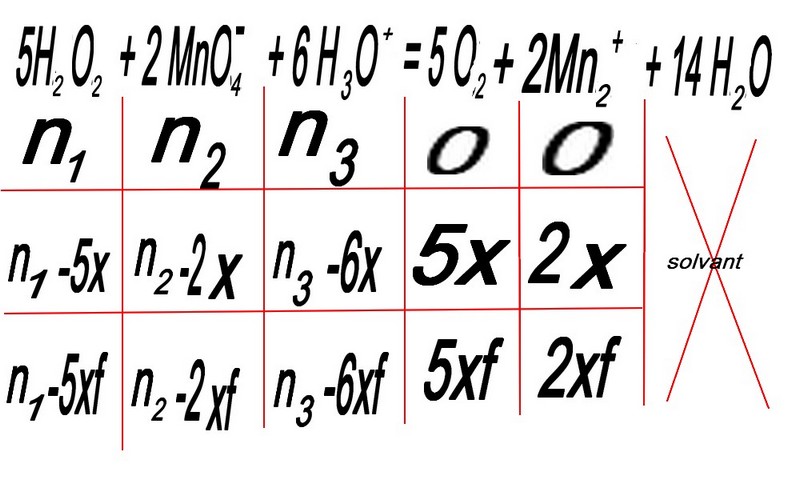Inscription / Connexion Nouveau Sujet
Determination de la valeur réelle de la Concentration de H2O2
Bonjour J'ai un gros devoir de chimie a rendre pour mardi et j'ai un soucis sur une partie pourriez vous m'aider?
Pour vérifier la valeur de la concentration de H2O2 établie à C[h2O2]=0.8 mol/L, on réalise le titrage d'un volume V0= 10.0mL de cette solution par une solution de permanganate de potassium acidifiée de concentration en soluté C1= 2.0*10-1mol/L. Les couples oxydant/reducteur intervenant sont MnO4-[sup]/ Mn[sup]2+ et O2/H2O2 . Le volume de permanganate de potassium versé pour obtenir l'équivalence est Veq=14.6mL
L'équation de rédaction et la suivante :
5H2O2 + 2 MnO4-[sup] + 6 H3O+ = 5 O2 + 14 H2O
QUESTIONS :
2.2. Quelle relation peut-on écrire entre la quantité initiale de H2O2 se trouvant dans le bécher n0(h202) et la quantité d'ions permanganate introduits dans le becher a l'équivalence neq(Mn04-)?
2.3. Donner l'expression de la concentration en H2O2de la solution commerciale [H2O2] en fonction de C1, V0 et Veq .
2.4. Montrez que l'on a [H2O2]exp = 7.3*10[sup]-3mol/L
2.5. Comparer C[H202]= 0.8 mol/L. Les erreurs de manipulation mise à part, comment peut-on expliquer l'écart de concentration obtenu ?
Pourquoi le ciel est bleu ?
Alors, il était une fois à la création de la Terre, ... bla ... bla ... bla
=> mauvaise feinte 
les correcteurs qui floodent ,quel abus de droit je vous jure , vous ne montrez pas l'exemple
/reprends l'avantage
Un membre important (parmi le top 10) qui a négocié pour faire le magnétisme et les dosages pour ne pas en accoucher une au bout de 2 mois, ne montre pas l'exemple à ceux qui vont concevoir des fiches à l'avenir.
\reprends l'avantage 
Oui je suis la en réalité toute les questions faites je ne l'ai pas mise
je bloque surtout sur la 2.1 !
heu, il n'y a pas de 2.1 ...
QUESTIONS :
2.2. Quelle relation peut-on écrire entre la quantité initiale de H2O2 se trouvant dans le bécher n0(h202) et la quantité d'ions permanganate introduits dans le becher a l'équivalence neq(Mn04-)?
2.3. Donner l'expression de la concentration en H2O2de la solution commerciale [H2O2] en fonction de C1, V0 et Veq .
2.4. Montrez que l'on a [H2O2]exp = 7.3*10[sup]-3mol/L
2.5. Comparer C[H202]= 0.8 mol/L. Les erreurs de manipulation mise à part, comment peut-on expliquer l'écart de concentration obtenu ?
oui mais je devrai , d'après l'énoncé trouver 7.3*10^-1 mol.L au lieu je tombe sur 2.92*10^-1 mol.L
c'est pas bon
C'est Bon j'ai enfin trouvé !!
A l'équivalence les quantités de matière des réactifs mis en présence sont en proportions stoéchiomètriques, donc :
neq(MnO4-) -2xéqui=0 donne : xéqui= ½neq(MnO4-)
n0(H2O2)-5xéqui=0 donne n0(H2O2)=5xéqui=2,5 neq(MnO4-)
n0(H2O2)=2,5 neq(MnO4-).
neq(MnO4-) = c1 Veq=2,0 10-1 * 14,6 10-3 = 2,92 10-3 mol.
n0(H2O2)= 2,5*2,92 10-3 = 7,3 10-3 mol
[H2O2]exp=n0(H2O2)/ V0= 7,3 10-3/ 10,0 10-2 = 7,3 10-1 mol/L.
merci quand meme pour votre aide , tant qu'aux autres mon tuto été trés serieux pas besoin de vos discution personnel!

 !
!