Inscription / Connexion Nouveau Sujet
determination d'un taux d'avancement final par conductimétrie
Bonjours à tous, voila j'ai un beau devoir maison à rendre, et j'ai un exo magnifique où je vous demande de m'aider...
Voici l'enoncé
On souhaite déterminer la consante d'acidité du couple acide acétique/ion acetate à l'aide d'une mesure conductimetrique.
On appelle constante de cellule k le rapport de la conductance G et de la conductivité de la solution  .
.
On peut donc écrire la relation : G=K .
.
Dans les conditions de l'experience, la constante de celule vaut k= 2,5x10^-3 m.
Dans un becher, on verse un volume Vo= 100 mL d'une solution So d'acide acétique, de concentraion molaire apportée co = 1,00x10^-3 mol/L. On immerge la cellule d'un conductimetre. Celui ci mesure une conductance de valeur G= 11,5 microS.
On note  la conductivité molaire ionique de l'ion oxonium H3O+ et
la conductivité molaire ionique de l'ion oxonium H3O+ et  ' la conductivité molaire ionique de l'ion acetate CH3CO2-.
' la conductivité molaire ionique de l'ion acetate CH3CO2-.
Données:
On rappelle l'expression de la conductivité  en fonction des concentrations effectives des especes ioniques Xi en solution :
en fonction des concentrations effectives des especes ioniques Xi en solution :
 =
= 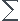
 i[Xi]
i[Xi]
Conductivités molaires ioniques à 25°C (conditions de l'experience)
 = 3,5x10^-2 S.m².mol^-1
= 3,5x10^-2 S.m².mol^-1
 ' = 4,1x10^-3 S.m².mol^-1
' = 4,1x10^-3 S.m².mol^-1
Dans cette solution, la faible concentration des ions HO- rend négligeable leur participation à la conduction devant celle des autres ions.
1) La conductance de la solution est elle changée si on modifie l'un des parametres suivant en gardant les autres identiques:
a. la concentration apportée co;
b. le volume Vo de la solution;
c. la temperature de la solution.
Pour chacun des parametres, justifier la reponse.
2) Ecrire l'equation de la reaction modelisant la transformation entre l'acide acetique et l'eau.
3) Donner l'expression du quotient de reaction à l'equilibre Qreq associé à l'equation precedente et en deduire une relation entre l'avancement final Qreq, xfinal, co et Vo.
4) Donner l'expression de G, conductance de la solution et en deduire une relation entre G et l'avancement final xfinal. Calculer la valeur de xfinal en mol.
5) Calculer le taux d'avancement final. La transformation peut elle être considerée comme totale ?
Voila, j'espere que vous pourrez maider. Je vous remercie d'avance et vous souhaite un Joyeux Noel !

Bonjour, (et Noyeux Joël bien sur...)
As-tu quelques idées pour chaque question?
ques1) voir ton cours (de quels paramètres dépend la conductance?)
la conductivité d'une solution électrolytique augmente si la concentration des especes chimiques presentes dans cette solution augmente.
la conductivité d'une solution électrolytique augmente si la temperature dans cette solution augmente.
mais je ne sais pas comment justifier ca... je peux pas mettre juste les phrases XD
Bonjour,
1) commence par écrire la conductiviité en fonction des espèces présentes et des conductivités molaires ioniques.
Comme G = k, si
varie, G aussi. Demande toi alors:
a. est-ce que la conductivité change quand tu fais varier co?, vo? (sous entendu est-ce que les concentrations ioniques changent?)
c. les conductivités molaires ioniques dépendent de la température (c'est pour ça que celles qui sont fournies dans l'énoncé précisent "à 25°C" )
2) réaction acido-basique mettant en jeu les couples CH3COOH/CH3COO- et H3O+/H2O
3) définition du cours pour le quotient de réaction.
Fais un tableau d'avancement pour trouver la relation, et remplace les concentrations dans l'expression du quotient de réaction à l'équilibre par xf, co et Vo.
4)G= k , exprime la conductivité à l'aide des concentrations de CH3COO- et H3O+ et exprime ces concentrations en fonction de xf grace à ton tableau d'avancement
résultat: xf= GVo/ k ()
5) Si la réaction était totale, on aurait xmax = coVo = ... (je te laisse faire le calcul)
...
si est inférieur à 100%, la réaction n'est pas totale.
Je n'ai volontairement pas répondu aux questions mais juste donné les pistes, par contre si tu postes ce que tu as fait, et ce que tu n'as pas compris je te répondrai sans aucun problème. Pareil si tu veux d'autres indications. 
Joyeux noël au passage 
PS: "un exo magnifique"  :D
:D
ques1) ce que tu dis est exact mais on te demande de JUSTIFIER...(trop facile sinon...) :
- La conductivité d'une solution électrolytique augmente si la concentration des especes chimiques presentes dans cette solution augmente car si on a plus d'ions entre les plaques de l'électrode ca engendre quoi ?...
- La conductivité d'une solution électrolytique augmente si la temperature dans cette solution augmente car l'agitation thermique engendre quoi?
-Pour le volume?
ques2) ?
jcomprend pas ce que je dois mettre XD
si on a plus d'ions entre les plaques de l'électrode ca engendre quoi ?...
ya plus de conductivité XD
l'agitation thermique engendre quoi?
plus de reaction
franchement je suis perdu XD
tu dis :
- "si on a plus d'ions entre les plaques de l'électrode ca engendre quoi ?...ya plus de conductivité" : oui c'est ca donc le courant entre les 2 plaques est plus important...
- "l'agitation thermique engendre quoi? plus de reaction?" tu parles de réaction chimique? ou de chocs sur les plaques? c'est juste que lorsque la température augmente, les ions seront plus mobiles donc le courant passera beaucoup plus vite entre les plaques...
merci beaucoup ! je vais voir si j'arrive a faire avec les "pistes" :p
sinon je demande votre aide !
merci beaucoup et joyeux noel !!!
le PS etait ironique jespere :p
bonjour, XD
alors voila j'ai fait tout ce que vous m'avez dit.. le probleme : je bloque pour la 4
4) Donner l'expression de G, conductance de la solution et en deduire une relation entre G et l'avancement final xfinal. Calculer la valeur de xfinal en mol.
tu m'as donner le resultat.. donc j'ai essayer de le retrouver avec toutes mes relations etc. Mais j'arrive pas à mettre Vo et k en denominateur.. je deviens fou XD
Merci beaucoup
Voilà le tableau d'avancement:
CH3COOH + H2O = CH3COO- + H3O+
état final C0V0 - xf excès xf xf
on exprime G:
G = k
G = k( [CH3COO-]éq
 ' + [H3O+]éq
' + [H3O+]éq
 )
)
or [CH3COO-]éq = [H3O+]éq = xf/V0
G = k(  '+
'+ )
)
d'où
xf = G V0 / (k
V0 / (k (
( +
+ '))
'))
PS: je viens de remarquer que tu as dû mal lire l'expression que je t'ai donnée: Vo est au numérateur, pas au dénominateur! 
T'en sors tu?
Thetys. 
(oui, le ps de mon premier message était ironique  )
)
jdois etre autiste, en fait jme suis trompé en ecrivant vite XD bref merci beaucoup et bonne fin d'année ! jte remercie vraiment beaucoup !!!!



