Inscription / Connexion Nouveau Sujet
Contrôle par titrage
slt tlm j'ai un exercice à faire pour la rentrée(je suis encore en vacances ^^) et je bloque dessus dèq la première question si qqn pouvait m'aider ce serait super merci
On prépare une solution S d'acide chlorhydrique, de concentration cs=8,0.10-3mol.L-1, à partir d'une solution commerciale, dont l'étiquette porte les indications suivantes: "densité par
rapport à l'eau : d=1,18 ; pureté : p=35%".
1. Calculer le volume Vc de la solution commerciale à prélever pour préparer un volume V=1,0 L de solution S.
2.a. Enumérer le matériel nécessaire pour réaliser la dilution.
b. Décrire le mode opératoire.
3. Pour contrôler la concentration de la solution S,on titre un volume Vs=20,0mL de S, prélevé avec une pipette jaugée, par une solution aqueuse d'hydroxyde de sodium Na+(aq) + HO-(aq), de concentration c1 = 1,00.10-2mol.L-1.
L'équiavalence est obtenue par un volume Véquiv=16,4 mL.
En déduire la concetration recherchée.
4.a. L'incertitude relative sur la valeur de C1 est de 1%. les incertitudes absolues sur les valeurs respectives de Vs et de Véquiv sont de 0,06mL et de 0,05mL. Déterminer l'intervalle de confiance relatif à la valeur mesurée de cs.
b.La valeur théorique de cs appartient-elle à cet intervalle de confiance.
svp vous pouvait m'aider je n'y pige rien du tout, mais vraiment acune question.
surtout la 1 et toute la 2.
merci d'avance
pour la première question
à partir de la donnée d=1,18 on peut déduire que la masse de 1L de solution est 1180g
Cette solution ne contient que 35% de HCl,donc la masse de HCl dans 1L de solution est
m=1180*0,35=413g
laconcentration massique Cm est donc 413g/L
la concentration molaire C se trouve à partir de la formule (facile à mémoriser) Cm=C.M
Sinon
C=n/V =(m/M)/V=(m/M)/V=Cm/M
2)Je suppose que tu as déjà fait une dilution........
pour calculer le volume à prélever V1 de solution de concentration C1 pour préparer un volume V2 de concentration C2,on utilise la relation
C1V1=C2V2
3)écris l'équation de réaction
à l'équivalence CaVa =CbV(eq) soit Cs.V=C1.Veq
attention,ce n'est pas le C1 du 2)
4)Cs= (C1.Veq)/V
 Cs/Cs=
Cs/Cs= C1/C1 +
C1/C1 + Veq/Veq +
Veq/Veq + V/V
V/V
 C1/C1 est l'incertitude relative sur C1 elle vaut 0,01
C1/C1 est l'incertitude relative sur C1 elle vaut 0,01
 Veq est l'incertitude absolue sur Veq
Veq est l'incertitude absolue sur Veq
 Veq =0,06mL
Veq =0,06mL
Tu peux calculer l'incertitude relative sur Veq
Même chose pour V
Une fois trouvée l'incertitude relative sur Cs, tu en déduis  Cs
Cs
d'où
Cs- Cs
Cs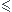 Cs
Cs 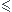 Cs+
Cs+ Cs.
Cs.
tu vérifies si la valeur Cs(théorique =donnée dans l'énoncé) se trouve dans


