Inscription / Connexion Nouveau Sujet
Conductivité et pH
Bonjour à tous, je souhaiterais votre opinion concernant un exercice traitant de la conductivité et du pH.
Voici l'énoncé :
"On dispose de 500 mL d'une solution (S) d'acide fluorhydrique HF (toxique) de concentration en soluté apporté c = 2,0.10^-2 mol.L-1.
Son pH est de 2,5 et sa conductivité  = 1,4.10^-1 S.m-1.
= 1,4.10^-1 S.m-1.
1.Le but de cette première partie d'exercice est de montrer que la réaction de l'acide fluorhydrique avec l'eau est une transformation chimique non totale.
a. Ecrire l'équation de cette réaction.
b. Quelle est la concentration en ions H3O+ de (S)?
c. Quelles seraient la concentration en ions H3O+ et la conductivité de la solution (S) si la transformation chimique était totale?
d. Montrer que les résultats précédents confirment que la transformation n'est pas totale.
2.On se propose dans cette deuxième partie d'étudier l'équilibre du système chimique.
a. Donner l'expression de la constante d'équilibre K pour l'équation écrite en 1.a.
b. Dresser un tableau d'avancement de la réaction.
c. En déduire l'avancement final de la réaction puis la valeur de K.
d. quel est le taux d'avancement final de la réaction?
e. Quelle est la composition de la solution (S) dans un état tel que l'avancement x = 1,0.10^-3 mol? Le système est-il alors à l'équilibre?"
Voilà mes réponses :
a. HF + H2O = F- + H3O+
b. [H3O+]=10^-2,5=3,2 x 10^-3 mol.L^-1
c. Si la transformation était totale : [H3O+]=c,  =8,1.10^-1 S.m^-1
=8,1.10^-1 S.m^-1
d. Concentration : Résultat de b. différent de celui de c. et conductivité du c. différente de celle de l'énoncé donc transformation non totale
C'est surtout à partir de là que ça pose plus problème :
2.a.K=Qr,f  K=([H3O+]f.[F-]f)/[HF]f (eau solvant donc on prend sa concentration égale à 1)
K=([H3O+]f.[F-]f)/[HF]f (eau solvant donc on prend sa concentration égale à 1)
b. Tableau
c. xf=[H3O+]f.V
 =[H3O+]f(
=[H3O+]f( H3O+ +
H3O+ +  F-) (car [F-]f=[H3O+]f=xf/V)
F-) (car [F-]f=[H3O+]f=xf/V)
Donc [H3O+]f= /(
/( H3O+ +
H3O+ +  F-)
F-)
donc xf =  /(
/( H3O+ +
H3O+ +  F-).V.10^-3
F-).V.10^-3
J'obtiens alors xf=1,7.10^-3 mol
Ensuite, d'après le tableau :
[HF]f= c - [H3O+]f donc
K=([H3O+]f.[F-]f)/(c-[H3O+]f) J'obtiens K=7,2.10^-1
d.Je trouve  =1,7.10^-1
=1,7.10^-1
e.Je ne sais pas trop ce que l'on attend de nous dans la première partie de cette question mais j'ai calculé les quantités de matière de chaque espèce en présence : Soit t la date à laquelle l'avancement est égal à 1,0.10^-3
(nHF)t=9,0.10^-3 mol
(nF-)t=1,0.10^-3 mol=(nH3O+)t
donc [HF]t=1,8.10^-2 mol.L^-1
[F-]t=[H3O+]t=2,0.10^-3 mol.L^-1
Je calcule alors Qr,t et je trouve Qr,t=2,2.10^-4. Comme Qr,t est différent de K j'en déduis que le système n'est pas à l'équilibre
J'ai des doutes concernant la fin essentiellement. Qu'en pensez-vous??
Merci d'avance
salut:
on doit vous donner :
 (H3O+)=34,98.10-3 S.m2/mol
(H3O+)=34,98.10-3 S.m2/mol
 (F-)=5,54.10-3 S.m2/mol
(F-)=5,54.10-3 S.m2/mol
a. HF + H2O = F- + H3O+ correct
b. correct
c. Si la transformation était totale : [H3O+]=c correct .
 =8,1.10^-1 S.m^-1 oui.
=8,1.10^-1 S.m^-1 oui.
en effet:
 =c.
=c.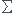
 =20mol/m3(40,52).10-3S.m2/mol=8,1.10-1 S.m-1
=20mol/m3(40,52).10-3S.m2/mol=8,1.10-1 S.m-1
d. Concentration : Résultat de b. différent de celui de c. et conductivité du c. différente de celle de l'énoncé donc transformation non totale . bien
---------------
2.a)
b) Tableau d'avancement:
or no(HF)=CV=2.10-2 mol/L.0,5L=0,01mol
HF + H2O = F- + H3O+
0,01 excès 0 0 état initial
0,01 -x=9m.mol excès x=1m.mol x=1m.mol état final
c.
Ensuite, d'après le tableau :
[HF]f= c - [H3O+]f donc
d.
e.si x = 1,0.10-3 mol
la composition de la solution (S) devient:
HF + H2O = F- + H3O+
0,01 excès 0 0 état initial
0,01 -x =9m.mol ... x=3m.mol x=3m.mol état final
<1
=>Le système n'est^pasà l équilibre. sauf erreur de calcul.
Merci de votre réponse  .
.
Je ne comprends pas pourquoi on ne trouve pas les mêmes resultats en utilisant la conductivité ou le pH... On n'obtient pas le même xf selon la méthode choisie.
Comment avez-vous complété cette ligne du tableau d'avancement : "0,01 -x=9m.mol excès x=1m.mol x=1m.mol état final" ?
Ne devrait-on pas plutôt avoir 8,4 mmol pour la quantité de matière de l'acide fluorhydrique à l'état final étant donné que xf=1,58.10^-3 mol ?
Vous obtenez xmax=0,01 mol pour le calcul du taux d'avancement en faisant c.V ?
Je ne vois pas non plus comment vous obtenez xf=3mmol dans le e.
oui tu as raison on ne trouve pas les mêmes resultats en utilisant la conductivité ou le pH.
normalement on doit trouver les memes résultats , car les mesures de PH et de la conductivité doivent etre faites au meme instant et lorsque l'équilibre est atteint .
mais avec la conductivité on trouve:dans
2)b)
xf= .V /
.V / 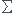

=1,4.10-1 S.m-1 .500.10-6 m3 / 40,52.10-3S.m2/mol
=1,7.10-3 mol  1,58.10-3 mol
1,58.10-3 mol
j'avais constaté ceci avant que tu me le dise , il faut voir celui qui a posé l'exercice.
e) je reprend si x = 1,0.10-3 mol=1m.mol
no(HF)=0,01 mol=10m.mol
la composition de la solution (S) devient:
HF + H2O = F- + H3O+10m.mol excès 0 0 état initial
10 -x =9m.mol ... x=1m.mol x=1m.mol état final
HF étant le réactif limittant => xmax=0,01mol
<1
la réaction n'est pas totale.
Ok je vois  . xmax=c.V=0,01 et on prend xf = 1,0.10^-3 comme dans l'énoncé.
. xmax=c.V=0,01 et on prend xf = 1,0.10^-3 comme dans l'énoncé.
Selon vous quelle est la méthode "préférable" entre celle du pH et de la conductivité? Il va falloir faire un choix de toute manière :/.
Désolé pour le double post mais êtes vous surs que c'est le taux d'avancement qu'il faut calculer pour montrer que le système n'est pas à l'équilibre?
Ne faudrait-il pas plutôt montrer que Qr,t (avec t la date à laquelle x=1,0.10^-3 mol) est différent de K la constante d'équilibre calculée précédemment?



