Inscription / Connexion Nouveau Sujet
Chromate d'argent
Bonjour Ilemathiens et Ilemathiennes, j'ai un problème avec ce petit exercice de Chimie.
J'aurais besoin de vos aides s'il vous plait pour savoir s'il est juste, merci.
_________________________________________________________________________________________________
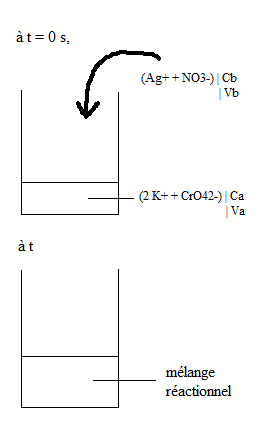
On mélange un volume VA = 50 mL de solution de chromate de potassium, 2 K+ + CrO42-, de concentration CA = 2,00.10-2 mol.L-1.
Et un volume VB = 50 mL de solution de nitrate d'argent, Ag+ + NO3-, de concentration CB = 4,00.10-2 mol.L-1. On observe l'apparition d'un précipité rouge
brique de chromate d'argent. On filtre le mélange obtenu et on récupère le précipité. Après rinçage et séchage, on obtient une masse de 0,21 g.
1. Déterminer les quantités d'ions argent et chromate dans l'état initial.
Comment qualifier un tel mélange ? Quel est l'avancement maximal de la réaction de précipitation ?
2. Déterminer l'avancement final et le taux d'avancement final de la réaction. Conclure.
3. Quelle est la composition en quantités de matière du système dans l'état final ?
Salut !
!
Ca me paraît bon Tu peux juste revoir les chiffres significatifs (faut bien trouver à redire qd c'est bon)
Tu peux juste revoir les chiffres significatifs (faut bien trouver à redire qd c'est bon)
"on en déduit que la réaction n'est pas totale mais presque".
Ca par contre, ça me paraît un peu limite... La réaction est quasiment totale
bonjour j'ai le même exercice mais pourriez-vous me dire s'il vous plaît qu'est ce qu'un mélange d'état d'équilibre svp ?
et pour les chiffres je penses qu'il suffit d'en mettre 2 non ?
Pa contre je n'ai pas compris la derniére question...pourriez vosu m'expliquer comment procéder ou comment il a fait sans tableau d avancement ?
merci
je dirais plutôt que le mélange est dans les proportions stoechoimétriques
pour la dernière questions les résultats sont fantaisistes
l'équation de réaction est
CrO42- +2 Ag+ = Ag2CrO4
l'avancement est
à une date t les qtés de matières valent
1.10-3-x 2.10-3-2x +x
comme x max =9.10-4 mol ,on peut calculer les qtés de matières restantes de CrO42- et Ag +
Les qté de K+ et NO[sub]3[sub]-[/sup]-[/sup] sont inchangées
merci de me répondre mais je ne comprend pas pourquoi x max = 9 .10^-4
Ce n'est pas plûtot 1.10^-3 ?
Donc on a les quantités de matiéres
Qu'est ce que ceci veut dire svp ?Les qté de K+ et NO[sub]3[sub]-[/sup]-[/sup] sont inchangées
merci 
Je retire ma derniére question mais quel réactif est limitant ?
Car on aura dans le tableau dans la case xmax
Pour CrO4 2- : 1.10^-3 - x max
Pour Ag + : 2.10^-3 - 2 xmax
donc pour les 2 on a 0 .On a donc une réaction totale or on toruve en xef =9,4.10^-4
non ?
Je trouve nf ( CrO4 2-) = 0,60.10^-4
nf ( Ag+) = 0,12.10^-4
nf (AgCrO4) = 9,4.10^-4
Est-ce cela svp???
si la réaction était totale,on aurait xmax=1.10-3 mol.
Or ,on nous dit que la masse de chromate d'argent recueillie est 0,21g.
La qté de chromare est donc n=m/M
j'ai utilisé ,sans le vérifier un résultat de calcul donné ci-dessus.
Or il y a une erreur.
le précipité a pour formule CrO4Ag2 soit M=52+64+2.107,8=331,6g
n=0.21/331.6=6,33.10-4mol
L'avancement réel est donc x=6,3.10-4mol
Cela est faible.On pouvait s'attendre à une réaction quasi totale car le chromate d'argent est très peu soluble dans l'eau.
Quelles sont les données de ton énoncé?
eh bien celles ci : On mélange un volume VA = 50 mL de solution de chromate de potassium, 2 K+ + CrO42-, de concentration CA = 2,00.10-2 mol.L-1.
Et un volume VB = 50 mL de solution de nitrate d'argent, Ag+ + NO3-, de concentration CB = 4,00.10-2 mol.L-1. On observe l'apparition d'un précipité rouge
brique de chromate d'argent. On filtre le mélange obtenu et on récupère le précipité. Après rinçage et séchage, on obtient une masse de 0,21 g.
Mais donc la réaction est incompléte et je toruve 0 et 0 pour les réactifs quand on a x max dans le tableau
quelque chose m'échappe!
si la réaction était totale,xmax serait égal à 1.103-mol
il se formerait donc 1.10-3mol de Ag2CrO4.
La masse obtenue serait
m=331,6g *0,001=0,33g .
Or on n'en obtient que 0,21g ............La réaction n'est donc pas totale.
X vaut donc 6,33.10-4
Mais cette valeur est trop faible compte tenu du fait que Ag2CrO4 est très peu soluble.
La quasi totalité des ions aurait du réagir.
donc ce résultat est faux ?
et pour cette question ?
3. Quelle est la composition en quantités de matière du système dans l'état final ?
Vous pourriez m aider ?
je suis embarassé avec la question 3.
pour la 4,j'ai déjà donné des indications.
Tout va dépendre de la valeur que l'on prend pour xmax
la qté de matière restante d'ions chromate est 1.10-3-xmax
la qté de matière restante d'ions Ag+ est 2.10-3-2xmax
la qté de matière de Ag2CrO4 est xmax
la qté de matière de K+ et NO3- n'a pas changé .Je te les laisse calculer
j'ai pris pour xef = 6,4.10^-4
Donc j'ai nAg =0
nCrO4 2- = 3,6.10^-4
nAg2CrO4 = 6,4.10^-4
n K+ = 1,00.10^-3
et n NO3- = 2,00.10^-3
c'est cela ?
Les réactifs sont introduits dans des proportions stoechiométriques :
donc xmax = ni(Ag+)/2 = ni(CrO42-) = 1,0.10-3 mol
A l'état final :
nf (Ag2CrO4) = m/M = xf (avancement final)
donc à l'état final :
nf(Ag+) = ni(Ag+) - 2xf = ...
nf(CrO426) - xf = .....
faute de frappe :
c'est
nf(Ag+) = ni(Ag+) - 2xf = ...
ni(CrO426) - xf = .....
en faisant les calculs, je ne vois pas où est le problème ...
oui mais xf est égal a 6,4.10^-4 ?
donc nf Ag+ =2.10^-3 - ( 2 x (6,4.10^-4)
= 7,2.10^-4
et nf CrO4 2- =3,6.10^-4
C'est ça ?
camo 2: rectification
xmax c'est bien 1.10-3,mais xfinal c'est 6,3.10-4mol.(si pas d'erreur de calcul)
c'est avec cette valeur qu'il faut résoudre la dernière question
gbm
le problème que je me pose c'est la validité de la valeur de xfinal=6,4.10-4mol.
Cele ne me parait pas compatible avec le Ks du chromate de potassium (1,7.10-12.
je sèche sur ton pb d'AO.Mais je vais encore chercher.Je manque totalement d'entraînement dans ce domaine
La produit de solubilité n'est valable qu'en début de précipitation.
K = Ca.Cb2 < Ks en effet ...
Il faudrait utiliser loi d'action de masse (thermochimie) pour espérer trouver le bon résultat
Coriolan et moi-même nous posions des questions hors-programme. Tes calculs sont justes
si xf = 6,33.10-4 mol.

pour gbm
j'avais posé
Ks=[Ag]2.[CrO42-]=1,7.10-12
n(Ag+)restant en solution=2.10-3 -2x pour (x=xf)
n(CrO42-=1.10-3-x
Ks=[n(Ag+)/Vt]2.n(CrO42-)/Vt
Ks= [(0,001-2x)2/0,12].(0,001-x)/0,1=1,7.10-12
je n'ai pas fait la résolution mais x semble <<6,3.10-4.
Les 0,21 g ont peut-être été choisis "au pif"
si vous êtes aussi forts en maths qu'en physique et prêts à aider un pauvre éléve alors j'ai un autre dm 
si ça vous interrésse :
https://www.ilemaths.net/forum-sujet-295716.html#msg2552173
hihi