Inscription / Connexion Nouveau Sujet
chimie et spéléologie
bonjour, j'aurais vraiment besoin d'aide sur cet exo. merci
Données :
- Temperature: 25°c soit T=298k -pression atmosphérique: Patm=1.02*105Pa; R=8.31 SI -masse molaire atomique: M(C)=12; M(O)=16, M(Ca)=40 g/mol -densité d'un gaz par rapport à l'air: d=M/29 où M est la masse molaire du gaz.
-loi des gazs parfaits: P.V=n.R.T (P en Pa, V en m3, T en K).
Dans un ballon, on réalise la réaction entre le carbonate de calcium CaCO3(s) et l'acide chlorhydrique (H30+ + Cl-).Le dioxyde de carbone formé est recueilli par déplacement d'eau dans une éprouvette graduée. un élève verse dans le ballon un volume Vs= 100mL d'acide chlorhydrique à 0.1 mol/L. A la date t=0, il introduit rapidement dans le ballon 2g de carbonate de calcium CaCO3tandis qu'un camarade déclenche le chronomètre. les élèves relèvent les volumes de CO2 dégagé au cours du temps. La pression du gaz est égale à la pression atmosphérique.
La réaction chimique étudiée peut être modélisée par l'équation :
CaCO3(s) + 2H3O+ = Ca2+ + C02(g) + 3H20(i)
1)calculer la densité par rapport à l'air du dioxyde de carbone. Dans quelles parties de la grotte est il susceptible de s'accumuler?
2) Déterminer les quantités de matières initiales de chacun des réactifs.
3) Dresser le tableau d'avancement de la réaction et en déduire la valeur Xmax de l'avancement maximum. Quel est le réactif limitant?
4)a) exprimer l'avancement X de la réaction à une date t en fonction de Vco2, T, Patm et R. calculer la valeur numérique à la date t=20s.
b) calculer le volume maximum de gaz susceptible d'être recueilli dans les conditions de l'expérience. la transformation est elle totale?
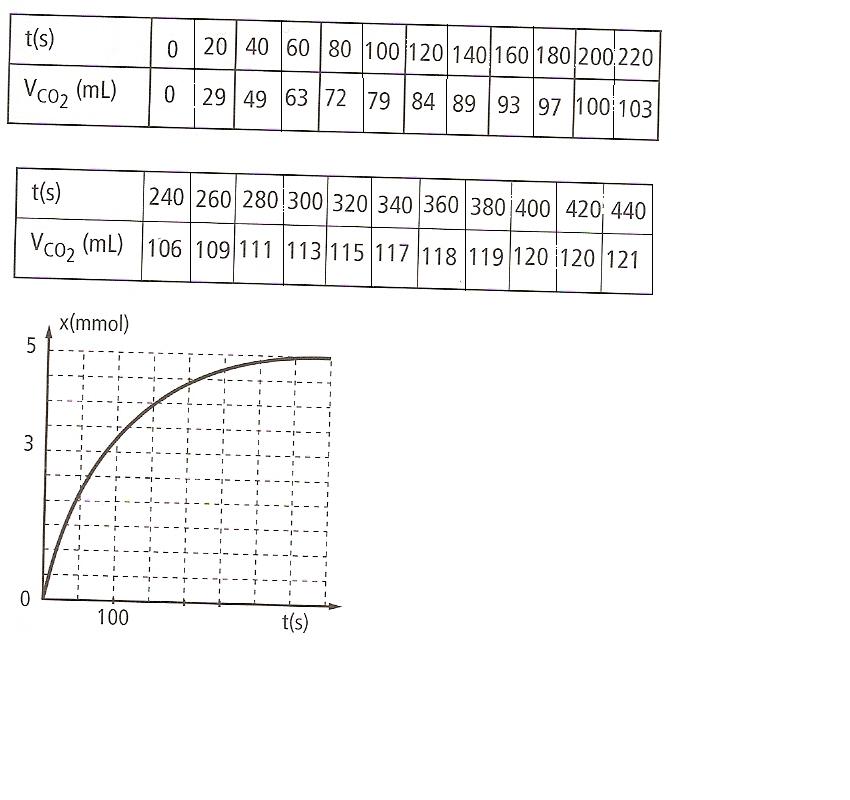
les élèves ont calculé l'avancement X et tracé le graphe suivant (voir plus bas)
5)a) donner l'expression de la vitesse volumique v de réaction en fonction de l'avancement et du volume Vs de la solution.
b)comment varie la vitesse volumique au cours du temps? justifier à l'aide graphe.
6) définir le temps de demi-réaction t(1/2). déterminer graphiquement sa valeur.
la température de la grotte qui doit être explorée par les élèves est inférieurs à 25°
7) quel est l'effet de cet abaissement de température sur la vitesse volumique de réaction à la date t=0?
8) tracer sur le graphe précédent l'allure de l'évolution de l'avancement en fonction du temps dans ce cas.
La réaction précédente peut être suivie en mesurant la conductivité  de la solution en fonction du temps.
de la solution en fonction du temps.
9)faire l'inventaire des ions présents en solution. Quel est l'ion spectateur dont la concentration ne varie pas ?
10) On observe expérimentalement une diminution de la conductivité  . justifier sans calcul ce résultat à partir des valeurs des conductivités molaires ioniques des ions à 25°c,
. justifier sans calcul ce résultat à partir des valeurs des conductivités molaires ioniques des ions à 25°c,
-  (H30+) = 35.0mS.m².mol-1
(H30+) = 35.0mS.m².mol-1
-  (Ca2+) = 12.0mS.m².mol-1
(Ca2+) = 12.0mS.m².mol-1
-  (Cl-) = 7.5mS.m².mol-1
(Cl-) = 7.5mS.m².mol-1
11) Calculer la conductivité  de la solution à la date t=0
de la solution à la date t=0
(les concentrations s'expriment en mol.m-3).
12) Montrer que la conductivité est reliée à l'avancement X par la relation:
σ = 4.25-580.x
13) Calculer la conductivité de la solution pour la valeur maximale de l'avancement.
1)utilise d=M/29
2)il n' y a pas de difficulté
3)tableau d'avancement classique
4)PV=nRt or ,dans ce cas n=x (avancement),donc on peut exprimer V en fonction de x
5) il suffit d'utiliser x=Xmax et de comparer avec V au bout de 440s
je n'ai pas vu la suite
1) M(Co2)=44 g/mol donc d=44/29=1.52
2) M(CaCO3)=100 g/mol n(CaCO3)i = m/M = 2/100=0,02 mol
c=n/v donc n=c*v n(H3O+)i=2(c*v)=2(0.1*100.10-3)=0.02 mol
3) Xmax=0.01 mol
c'est correcte pour les 3 premières questions ?
d(CO2)>d(air) ,donc le CO2 s'accumule dans les couches basses.
pourquoi n(H+)=0,02?
n=C*V=0,1*0,1=0,01 mol
à t=o n(CaCO3)=0,02 mol
n(H+)=0,01 mol (le coef 2 n'a pas sa place ici!)
à une date t
n(CaCO3)=0,02-x
n(H+)= 0,01-2x ( c'est ici qu'intervient le coef 2)
je reviendrais ce soir.
D'autres peuvent intervenir,évidemment!
ok, donc Xmax= 0.005 mol, le réactif limitant est H3O+ ?
4)a) il faut trouver la valeur de l'avancement x ou de Vco2 pour t=20 s ?
Xmax= 0.005 mol, le réactif limitant est H3O+
OK
il faut trouver la valeur de l'avancement x ou de Vco2 pour t=20 s
Il faut utiliser la loi des gaz parfaits : PV = nRT.
On a P, V, R, T ==> on peut trouver n (qui est égal à x).
Pour t = 20 s, on sait que VCO2 = 29 mL d'où n, donc x.
Oui, avec PV = nRT, on trouve 121,4 mL.
Cela correspond d'ailleurs à la valeur donnée (la dernière) dans la tableau.
5)a) V=1/Vs*(dx/dt).
5)b) v diminue au cours du temps
6) le temps de demi réaction est la durée nécessaire pour que l'avancement x soit parvenu à la moitié de sa valeur finale.
sur le graphe,on peut lire t1/2=60 secondes
est ce que ça va pour ces 3 réponses ?
C'est bon...
Une valeur plus précise de t1/2, obtenue par interpolation dans le tableau, est 56,4 s (parce que 63 n'est pas tout à fait la moitié de 121).
ok.
7) un abaissement de température entraîne une diminution de la réaction donc une diminution de la vitesse volumique de réaction.
8) il faut tracer la meme courbe sauf qu'elle sera en dessous de la 1ère
9) ions présents en solution: H3O+; Cl-; Ca2+.
l'ion spectateur est Cl-.
10)la variation de la conductivité est due seulement à la modification des concentrations de H3O+ et de Ca2+ puisque la concentration en Cl- ne varie pas. Au cours de la réaction, lorsque les 2 ions H3O+ disparaisent, 1 ion Ca2+ apparaît. comme la conductivité molaire des ions H3O+ est supérieur à celle des ions Ca2+, la conductivité diminue.
11) pour les concentrations, elles sont en mol.m-3 donc [H3O+]= [Cl-] =0,1mol/L =0,1.10-3 mol/m-3 ?
7) OK
8)
il faut tracer la meme courbe sauf qu'elle sera en dessous de la 1ère
Oui mais le maximum sera le même parce que xfinal ne dépend pas de la température mais du réactif limitant.
9) OK
10) très bien

11)
[H3O+] = [Cl-] = 0,1 mol/L = 0,1.10-3 mol/m3
Il y a au moins deux façons de trouver le résultat.
S'il y a 0,1 mol/L, 1 m3 étant 1000 fois plus grand qu'un litre, il y a 1000 fois plus de mol dans 1 m3 ==> 1000 x 0,1 = 100 mol/m3.
Il y a une autre façon qui a un avantage (==> on n'a pas besoin de réfléchir !
 ).
).
0,1 mol/L ==> il suffit de savoir que 1 L = 10-3 m3 et de remplacer.
0,1 mol/L = 0,1 mol/10-3 m3
(diviser par 10-3 revient à multipier par 103)
0,1 mol/L = 0,1 mol/10-3 m3 = 0,1.103 mol/m3 = 102 mol/m3
Ou :
0,1 mol/L = 0,1 mol.L-1 = 0,1 mol.(10-3m3)-1 = 0,1.103mol.m-3
(parce que (10-3m3)-1 = (10-3)-1(m3)-1 = 103m-3)
Donc 0,1 mol/L = 0,1.103 mol.m-3 = 102 mol.m-3
Mathématiquement, ce n'est pas très rigoureux parce qu'on fait des opérations sur des nombres et des unités mais ça a un avantage : on ne se trompe jamais...
Tu prends la méthode que tu préfères...
j'ai trouvé mais en fait il faut laissé les conductivité molaire ionique en mS.m2.mol-1 alors que lorsqu'on calcul la conductivité à t=0, elle sont converties en s.m2.mol-1
[Xi] est une concentration.
(0,01-2x) est une quantité de matière (nombre de moles) et V est donc le volume. (0,01-2x) / V est donc une concentration.
il faut laisser les conductivité molaire ionique en mS.m2.mol-1 alors que lorsqu'on calcule la conductivité à t=0, elle sont converties en S.m2.mol-1
C'est assez curieux !...
Je pense que tu n'as pas pris les bonnes unités...
Le volume V = 100 mL = 0,1 L = 0,1.10-3 m3 = 10-4 m3.
Et les
 i sont S.m2.mol-1
i sont S.m2.mol-1
Donc on a


