Inscription / Connexion Nouveau Sujet
Chimie
Bonjour, j'ai un dm de chimie pour la rentrée et j'ai trouvée à peu près les questions, mais je voudrais que vous me corrigiez et me dire si je peux rajouter quelque trucs si j'ai oublié de dire des choses et que vous m'aidiez au questions que je ne comprends pas. Merci de votre aide et bonne vacance pour ceux qui y sont =)
[b]DOCUMENT
Présentation:
Les hommes ont su très tôt utiliser les propriétés de quelques composés organiques. Dans
l'Antiquité, les Égyptiens, les Grecs, puis les Romains ont extrait des substances organiques
naturelles comme la pourpre d'un coquillage, le murex, l'indigo d'une plante, l'indigotier, afin de
les utiliser comme colorants. Au Moyen Âge, on obtient l'éthanol (alcool) par distillation du vin. Au
XVIe siècle, on extrait l'acide formique par distillation de fourmis, pour l'utiliser comme détergent.
Certaines transformations chimiques, encore utilisées actuellement sans trop de modifications, sont
également connues depuis l'Antiquité. On peut citer la transformation des graisses animales en
savon ou encore l'obtention d'alcool à partir de la fermentation d'amidon et de sucres. Si les
composés organiques étaient connus depuis longtemps, de quand date réellement la chimie
organique en tant que science ?
Document 1 : La naissance de la chimie organique
Doc 1: image 1
La chimie organique est une science jeune, dont l'origine est l'étude des substances naturelles
élaborées par les êtres vivants. Elle voit le jour au XVIIIe siècle en Allemagne et en France.
L'apothicaire Carl Scheele isole vers 1787 un certain nombre d'espèces chimiques organiques
naturelles et essaie d'en identifier les composants. Son contemporain, Antoine Lavoisier, imagine
une méthode de combustion permettant l'analyse chimique d'un composé. En 1807, le Suédois Jons
Berzélius baptise du nom de composés organiques les espèces chimiques provenant d'un matériau
d'origine vivante. Au début du XIXe siècle, les chimistes, qui disposent d'un matériel de laboratoire
de plus en plus performant, isolent de nombreux composés organiques comme l'acide citrique,
l'acide lactique, la morphine. Mais aucun n'en réalise la synthèse.
A cette époque, la chimie organique était surtout imprégnée d'idées
philosophiques: on pensait que les substances naturelles ne pouvaient être
reproduites par synthèse chimique. Leur élaboration semblait requérir
l'intervention d'une mystérieuse force, la «force vitale », inaccessible aux
scientifiques. On estimait que cette «force vitale » distinguait le monde
animal et végétal du monde minéral, celui du sol et du sous-soI.
La théorie de la « force vitale » prévalut jusqu'au XIXe siècle. Elle subit un
dur revers avec la découverte tout à fait fortuite du chimiste allemand
Friedrich Wolher, en 1828. En chauffant une solution de cyanate
d'ammonium, un réactif minéral, il obtint de l'urée en tout point identique à
celle extraite de l'urine des mammifères par Rouelle le Jeune dès 1773. La
synthèse de l'urée donna alors le grand élan. En effet, Wolher venait de
synthétiser un composé organique, à partir d'un composé qui ne l'était pas et
ce, sans l'intervention d'un organisme vivant.
Document 2 : Les progrès de 1835 à nos jours
Doc 2: image 2
À partir de 1835 se développent des méthodes d'analyse très poussées des composés organiques.
Des chimistes comme Louis Gay-Lussac et Jean-Baptiste Dumas à Paris, Jons Berzélius à
Stockholm déterminent la composition d'espèces organiques, en termes non seulement de nature
mais également de proportions des éléments présents. Les chimistes savent maintenant écrire la
formule chimique brute d'une espèce organique: elle est principalement constituée d'atomes de carbonne C, d'hydrogène H, plus rarement d'atomes d'oxygène O, d'azote N et d'halogènes (F, Cl, Br et I) enfin interviennent ponctuellement d'autre éléments comme Mg, Ca, ect...
Par contre, ils se heurtent à un problème: la structure des molécules, c'est-à-dire l'arrangement des
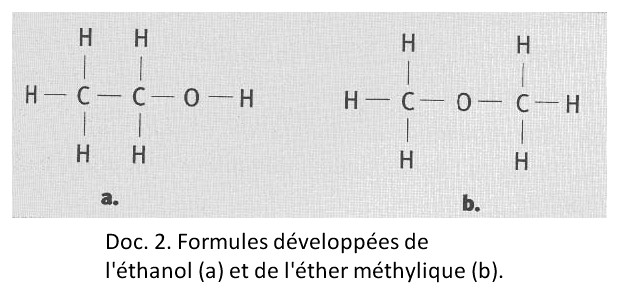
atomes entre eux. À l'époque, par exemple, les chimistes connaissent deux composés différents
répondant à la formule brute C2H60: l'alcool éthylique ou éthanol, dont la température d'ébullition
dans les conditions ordinaires est de 78 °C, et l'éther méthylique, gazeux. Comme ils n'ont aucune
notion sur la structure des molécules, ce fait reste très mystérieux. En 1830, Berzélius introduit la
notion d'isomérie pour distinguer des substances différentes de compositions identiques en
éléments.
En 1856, William Perkin synthétise le premier colorant: la mauvéine. C'est le début de la chimie
des colorants. Des efforts considérables sont déployés par de brillants esprits comme Edward
Frankland à Manchester, Berzélius, Dumas pour mettre en place le concept de la liaison de
covalence. Ce n'est qu'en 1858 qu'August Kékulé, à Heidelberg (Allemagne), et Archibald Scott
Couper à la Sorbonne proposent la première représentation d'une molécule par un groupe d'atomes
liés entre eux par des liaisons de covalence. Puis, vers 1875, s'élabore l'idée que les molécules se
développent dans l'espace avec le Néerlandais Jacobus Van't Hoff et le Français Louis Pasteur.
Les progrès deviennent alors extrêmement rapides, accélérés par la théorie quantique édifiée dans
les années 1920 et les méthodes d'analyse des molécules, qui ne cessent d'être améliorées au cours
du XXe siècle.
On peut citer quelques dates importantes, parmi d'autres :
1902 - synthèse de glucides par l'Allemand Emil Fischer;
1929 - synthèse d'un constituant de l'hémoglobine par l'Allemand Hans Fischer ;
1953 - détermination de la structure de l'ADN par le Britannique Francis Crick et
l'Américain James Watson ;
1973 - synthèse de la vitamine B12 par l'Américain Robert Woodward ;
1985 - découverte des fullerènes, molécules en forme de sphères, comportant 60 atomes de
carbone, par le Britannique Harold Kroto.
QUESTIONS
a) Quelles sont les substances étudiées en chimie organique au XVIIIe siècle?
b) Rappeler la définition d'une formule brute
c) Rechercher les formules brutes de l'acide citrique, l'acide lactique, l'urée et la morphine.
d) Qu'ont en commun ces molécules?
e) A notre époque, comment peuvent être définies les molécules appartenant à la chimie organique?
f) Comment et qui a permit d'expliquer la notion d'isomères?
g) Définir la notion d'isomères
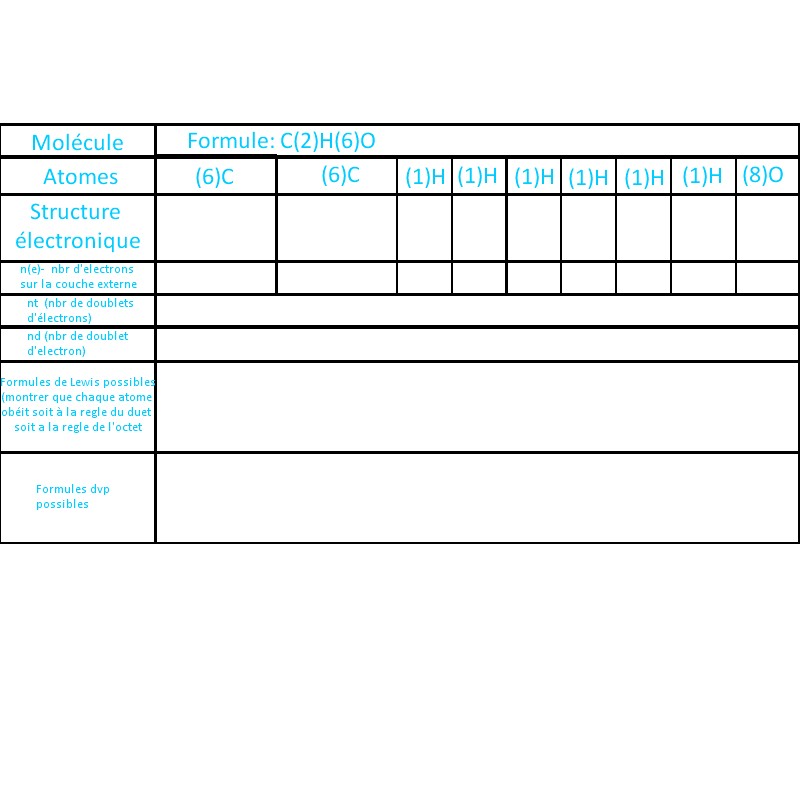
h) Utiliser le tableau 1 comment en seconde pour expliquer pourquoi un même composé de formule brute C₂H₆O possède deux formules développées.
i) La synthèse de la mauvéine par Perkins, en 1856, fut un moment privilégié de la chimie organique, pourquoi?
j) Comment Pasteur et Van't Hoff ont-ils perçus l'arrangement atomique de la plupart des molécules organiques?
k) Pour quelles raisons, les progrès de la chimie organique se sont-ils accélérés au cours du XXe siècle?
RÉPONSESles réponses soulignées sont celles que je ne comprends pas vraiment.
a) les substances sont: l'acide citrique, l'acide lactique, la morphine, la solution de cyanate d'ammonium, l'alcool éthylique, l'éthanol, l'éther méthylique, la mauvéine, le glucide, l'hémoglobine, la vitamine B12 et le fullerène.
b) La formule brute nous renseigne sur la composition de la molécule. Elle est la plus compacte et elle contient le moins d'informations qui s'écrit sous la forme C(x)H(y)O(z). Elle indique la nature et le nombre des atomes constitutifs et permet de calculer la masse molaire de la molécule.
Ex: Éthanol C(2)H(6)O
c) Acide citrique: C(6)H(8)O(7)
Acide lactique: C(3)H(6)O(3)
Urée: CH(4)N(2)O
Morphine: C(17)H(19)NO(3)
d) Elles ont toutes les quatre composées d'au moins un oxygène, un carbone et un hydrogène.
e) Je n'ai pas trouvé.
f) Je dirais que c'est Edward Frankland, Berzélius Dumas, August Kékulé, et Archibald Scott qui a permit d'expliquer la notion d'isomère mais je n'ai pas trouvé dans le texte comment.
g) Des isomères sont des composés qui ont la même formile brute mais des formules développées différentes. Ces sont des composés qui n'ont ni les mêmes propriétés physiques ni les mêmes propriétés chimiques. Exemple: pour le composé de formule brute C(3)H(6)O, il existe deux formules développées possibles, Propanal et Propanone.
h) Pour le tableau, je ne comprend pas pourquoi il y a autant d'atome en faite et je ne me rappelle plus exactement comment on doit s'y prendre pour le remplir, donc si vous pourriez m'expliquer ce tableau se serai gentil =)
i) C'était un moment privilégié de la chimie organique car c'est la première étape de la chimie des colorants.
j) je ne la comprend pas tellement.
k) Car il y a des découvertes de différentes synthèses et les isomères notamment avec la formule de Lewis fait avant la chimie organique.
 MERCI DE VOTRE AIDE!
MERCI DE VOTRE AIDE!

quel boulot de recopier tout cela!
e)les molécules appartenant à la chimie organique sont les composés du carbone (à l'exception de CO CO2 les carbonates les cyanures les carbures ,considérés comme composés minéraux)
f)Berzelius introduit la notion d'isomères à partir de la différences de propriétés de l'éther et de l'alcool éthylique
h) tableau :les nombre entre parenthèses désignent le numéro atomique
par exemple ,pour (6)C la configuration est K2 L4 soit 4 électrons sur la couche externe.
en fait on a fait l'inventaire des atomes constituant la formule C2H6O
je suppose qu'on fait la distinction entre doublets totaux et liants
nt et nd ne sont pas clairement définis dans le tableau
on te donne les formules développées.Il suffit de rajouter les doublets non liants sur l'atome d'oxygène
pour montrer que la règle de l'octet (ou du duet ,pour H) sont safisfaites ,il suffit de faire un cercle entourant un atome et les tirets(=doublets)qui y sont rattachés.utilise plusieurs couleurs pour que ce soit plus clair
Pasteur et Van 't Hoff ont compris que les atomes des molécules organiques ont une distribution spatiale,c'est à dire qu'elles sont arrangées dans les 3 dimensions de l'espace.
Merci de votre réponse. Pour les questions précédentes j'avais juste?
Je ne vais pas vous mentir, j'ai trouvé le texte du TP sur internet, c'était donc plus facile =)
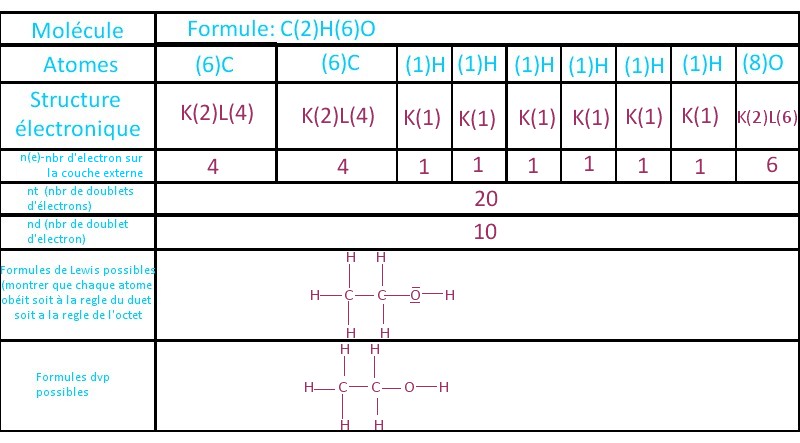
Pour le tableau, excusez-moi mais je me suis trompée pour nt et nd, nt est le nbr total d'électron et nd est le nbr de doublet d'électrons. J'ai rectifié.
Par compte je ne comprends pas votre cercle qu'il faut faire pour montrer que chaque atome obéit à soit à la règle du duet soit à la règle de l'octet.
Merci.
Bonjour, vous pouvez me répondre s'il vous plaît  même si je sais que c'est le weekend ^^
même si je sais que c'est le weekend ^^
Bon dimanche.

OK pour les réponses
pour d) écrire elles sont...
pour le tableau rajouter la formule de l'éther ,isomère de l'éthanol.
pour justifier que la règle de l'octet ou du duet on peut répondre ainsi.
pour les atomes H:une seule liaison part de ces atomes (deux électrons): règle du duet vérifiée
pour les atomes C :4 liaisons partent de ces atomes.(8 électrons)
pour l'atome O: 2 liaisons partent de l'atome et il y a 2 doublets non liants soit au total 8 électrons.


