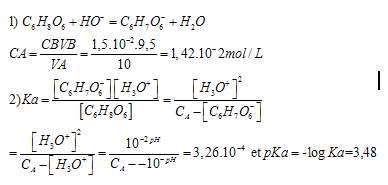Inscription / Connexion Nouveau Sujet
acide ascorbique
Bonsoir à tous,
je sollicite votre aide pour l'exercice que voici :
L'acide ascorbique, de formule brute C(6)H(8)O(6) peut être assimilé à un acide carboxilique de formule AH. Il réagit de façon limitée avec l'eau.
On dissout un comprimé d'acide ascorbique dans un peu d'eau distillée et on complète de manière à obtenir une solution S, de volume Vs = 200mL. On prélève alors un volume Va = 10.0mL de solution S, que l'on titre avec une solution aqueuse d'hydroxyde de sodium, de concentration cB = 1.5*10^-2, en présence d'un indicateur coloré approprié, le rouge de crésol. L'équivalence est obtenue pour un volume de soude versé Vequiv = 9.5 mL.
1. Ecrire l'equation chimique de la réaction de titrage et déterminer la concentration Ca en acide ascorbique de la solution S.
ma réponse : equation ???
cA*vA = cB*vB
cA = cB*VB/Va
cA= (1.5*10^-2)* (9.5*10^-3)/(9.5*10^-3)
cA = 1.5*10^-2 mol/l
2. Le pH de cette solution S est égal à 2.7 à 25°C. Déterminer les concentrations des espèces présentes dans la solution. En déduire le pkA du couple acide ascorbique/ ion ascorbate.
ma réponse : [AH] = xeq/V = 10-pH/V = 10^-2.7/10*10^-3
= 1.9*10^-1 mol/L
autres concentrations??
pKa = -log(kA)
mais je ne peux calculer kA sans l'equation de la reaction
merci d'avance