Inscription / Connexion Nouveau Sujet
notation inconnue
Bonsoir !
Dans un exercice sur la fragmentation par ionisation électronique (spectro, je suis tombée sur cette notation (en pj)... qui m'est complètement inconnue ... Que signifie le + et le point entourés ?
En vous remerciant par avance !
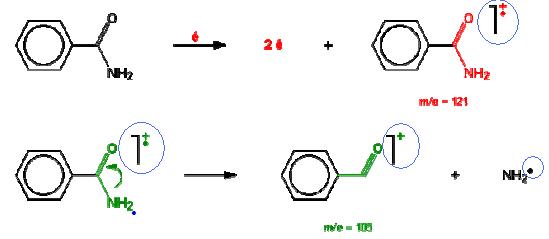
Bonsoir Nanalee13 :
C'est la perte d'un électron qui est la cause de l'ionisation d'une molécule . L'ion moléculaire est donc une espèce radicalaire . Un tel ion , ayant un électron non aparié , qu'il soit moléculaire
ou fragment est appelé un ion à nombre impair d'électrons , et se distingue par le symbole (+. ) . Lorsque l'on explique et que l'on classe les réactions de décomposition , il est souvent plus
pratique et plus facile de distinguer ces ions radicaux des ions à nombre pair d'électrons qui sont ceux dans lesquels les couches électroniques superficielles sont totalement garnies .
Les espèces cationiques radicalaires existent aussi mais sont moins stables. Ils apparaissent principalement en spectrométrie de masse. Lorsqu'une molécule en phase gazeuse est soumise à
Une ionisation électronique. Un électron est arraché par un électron du faisceau électronique, créant un cation radicalaire M+. Cette espèce dérive de l'ion moléculaire ou ion parent et indique
la masse moléculaire. Dans un spectre de masse typique, plus de signaux apparaissent en raison de la fragmentation de l'ion moléculaire en mélange complexe d'ions et de radicaux non
chargés. Ainsi par exemple, le cation radicalaire éthanol se fragmente en cation méthyle CH3+ et radical hydroxyle. Pour le naphtalène, le cation radicalaire non fragmenté est de loin le pic le
plus important du spectre. Les espèces secondaires sont générés par un gain (M+1) et une perte (M-1) en proton.
Bonnes salutations .


