Inscription / Connexion Nouveau Sujet
Transports ioniques
Bonjour, étant actuellement en PACES je m'entraine grâce à certains QCM sur mon chapitre Transports Ioniques mais je me retrouve face à une impasse.
En effet, on nous dit que :
Soit deux compartiments (1 et 2) contenant de l'eau, séparés par une membrane dialysante. On introduit dans le compartiment 1 :
- 0,1 mol.L-1 de protéine neutre
- 125 mmol L-1 de NaCl
La protéine est non diffusible au travers de la membrane, Na+, Cl- et l'eau étant diffusibles au travers de la membrane.
On donne : V1 = V2 = 5 litres, T = 300K, R = 8 USI
Et on nous demande de calculer la différence de pression osmotique entre les deux compartiments (j'ai la réponse qui est de 2.4 x 10^5 Pa mais pas les détails de la correction).
Ce que je ne comprends pas c'est si on doit calculer la différence de pression osmotique de NaCl ou en comptant aussi H2O.
De plus, dans mon cours la seule formule indiquée est celle de la différence de potentiel : V2-V1= (R.T)/F x ln(m1/m2)
En précisant que pour les cations c'est bien : m1/m2 , ce qui est différent pour les anions : m2/m1.
Merci d'avance si vous pouviez m'éclairer.
Bonjour emipaces
renseigne ton profil s'il te plaît conformément à
 extrait de
extrait de Q12 - Dois-je forcément indiquer mon niveau lorsque je poste un nouveau topic ?
Je te remercie

Bonjour,
1- Il s'agit bien de pression osmotique pas de ddp
2- Il n'y a qu'une pression osmotique, celle de la solution
3- je suppose que l'on demande la pression à l'équilibre (une fois NaCl diffusé)
Dans ce cas, vous devez avoir dans votre cours une formule connue puisqu'elle ressemble à la loi des gaz parfaits : 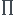 =cRT
=cRT

 équivalences des systèmes de niveaux scolaires
équivalences des systèmes de niveaux scolaires
