Inscription / Connexion Nouveau Sujet
thermo
bonjour,
je reviens encore avec de la thermo, ayant pas mal de difficulté il faut que je travail cette matiere.
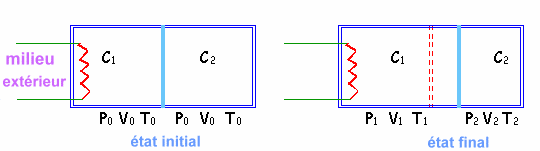
Un cylindre adiabatique est divisé en deux compartiments (I) et (II) par un piston, imperméable à la chaleur, pouvant se déplacer sans frottement.
A l'état initial, chaque compartiment contient une mole d'un gaz parfait, sous les mêmes conditions de pression de température (P0 et T0).
Le compartiment (I) contient une résistance électrique de capacité thermique négligeable. On chauffe le gaz du compartiment (I). A l'état final la température du gaz dans le compartiment (II) est égale à T2.
1) Déterminer les conditions finales (P, V et T) sous lesquelles se trouve le gaz dans chacun des compartiments.
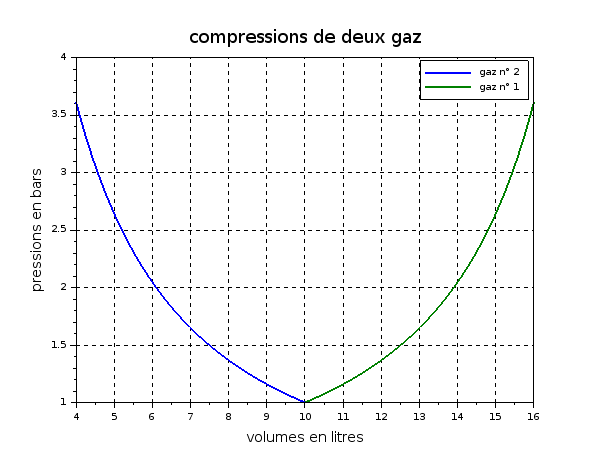
2) Tracer dans le plan (V, P) les deux transformations et indiquer la nature des transformations.
3) Déterminer pour chaque gaz la variation de l'énergie interne et le travail échangé : quelle est l'expression de la chaleur fournie par la résistance électrique ?
donc j'ai un schema qui correspond au fichier joint
en 1) je sais que PV=nRT donc P0V0=nRT0
n=1 donc P0V0=RT0 et P2V2=RT2
Le compartiment (II) subit une transformation adiabatique soit PVy=CSTE avec y=5/3 ou 7/5 selon la nature du gaz
je me retrouve avec P2= P0(V0/V2)y
V2=(P0/P2)1/y
T2=(P0/P2)(1/y)-1
V1=2V0-V2
T1= T0(P1V1/P0V0)
P1=(T1/T0)(V0/V1)P0
normalement si j'ai pas fait d'erreur, la question 1 est bouclé
La question 2):
pour le compartiment 2 pas de soucis, transformation adiabatique, je fais le graphe .
Par contre pour le compartiment un quel est la nature de la transformation? ce n'est pas adiabatique puisqu'il y a echange de chaleur, V,T et P ne sont pas constant non plus, du coup je seche
Merci pour votre aide
Bonjour
Tu peux déduire la courbe P=f(V) du gaz 1 de celle obtenue pour le gaz 2 : ma ession (donc l'ordonnée est la même mais le volume vérifie V1=2Vo-V2
faute de frappe : il faut lire "la pression" comme tu l'as sûrement deviné.
Petite précision : l'adjectif adiabatique s'applique à une transformation. Une paroi permettant une telle transformation, c'est à dire une paroi suffisamment bien isolée pour interdire les transferts thermiques est qualifiée d'athermane. Par opposition : une paroi très bonne conductrice thermique est qualifiée de diathermane.
bonjour vanoise
merci pour ta reponse.
effectivement il faut que je fasse attention a mes adjectif le jour de l'examen.
pour la courbe 2 je me retrouve avec quelque chose de la form (1/x)y avec y=5/3 ou 7/5
Pour la courbe de si je prend mon equation de P1 et que je remplace V1 par 2V0-V2 j'obtient une equation de la forme 1/(2-x) ca me parait bizarre.
Et je ne sais toujours pas quel est la nature de la transformation
La transformation du gaz n° 1 n'a pas de nom particulier. L'apport de chaleur n'est ni isochore ni isobare. P1 et V1 vérifient seulement les relations que je t'ai indiquées précédemment. Pour t'aider un peu concernant les courbes : voici une simulation sous Scilab pour deux gaz parfaits diatomiques (une mole de chaque) avec Vo=10L, Po=105Pa. L'état final du gaz n°2 correspond à un volume de 4L. Ces valeurs numériques sont totalement arbitraires mais cela te fournit l'allure des deux courbes.
Il est peut-être suffisant de faire remarquer que la courbe n° 1 est le symétrique de la courbe n° 2 par rapport à la droite verticale d'équation V=Vo.