Inscription / Connexion Nouveau Sujet
Solubilité minimale
Bonjour, je ne comprends pas bien la correction d'un exo sur la précipitation/dissolution en solution aqueuse. Voici l'énoncé :
"A une solution de Zn2+ à 1,0x10-3 mol/L, on ajoute de la soude sans variation de volume.
1. Décrire ce qu'on observe au fur et à mesure.
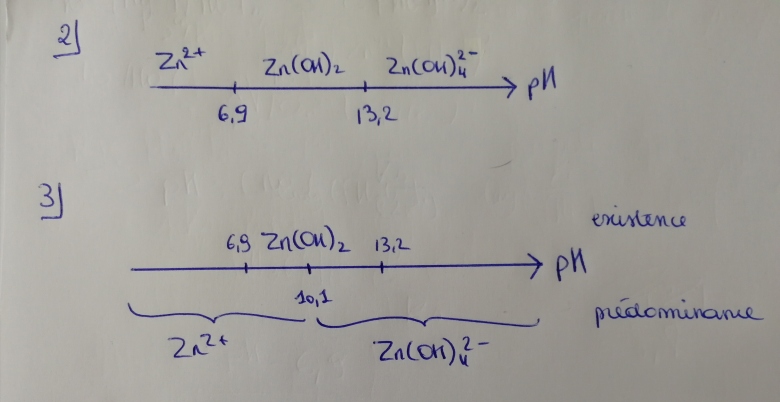
2. Etablir le diagramme d'existence du précipité.
3. Lui superposer le diagramme de prédominance des espèces solubles.
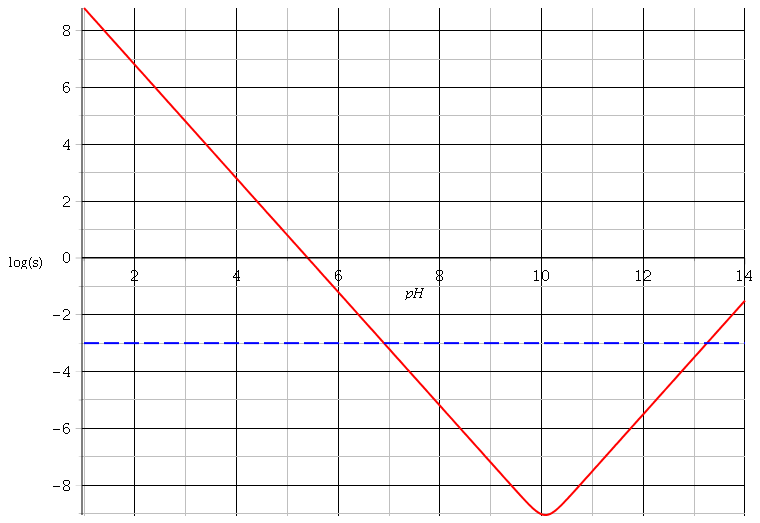
4. Déterminer le pH correspondant à la solubilité minimale de Zn(OH)2. Calculer cette solubilité.
Données : pKs(Zn(OH)2) = 17,2 // log(Zn(OH)42-) = 15,7
Je n'ai pas eu trop de soucis à faire les 3 premières questions :
1) Formation du précipité Zn(OH)2 puis disparition du précipité par formation du complexe Zn(OH)42-.
2) J'ai calculé les pH pour l'apparition et la disparition de Zn(OH)2 (je vous épargne les détails, les résultats sont justes et concordent avec la correction).
Vous trouverez le diagramme en annexe.
3) J'ai calculé le pH pour la limite Zn2+/Zn(OH)42-, je trouve 10,1 (là encore je vous épargne les calculs).
Vous trouverez le diagramme complété en annexe.
4 ) Pour la question quatre j'ai bloqué, je vois bien qu'il faut trouver une expression de la solubilité, la dériver en fonction de [H30+] afin de trouver le pHmin et smin mais je ne comprends pas la correction.
Elle dit simplement :
entre pH = 6,9 et 13,2  s = [Zn2+]eq + [Zn(OH)42-]eq
s = [Zn2+]eq + [Zn(OH)42-]eq
Je ne comprends pas comment on arrive à cette expression de la solubilité. Pourriez vous m'éclairer ? Merci d'avance.
Bonjour
la solubilité est la somme des concentration en ions zinc et en ions Zn(OH)42- quand ces ions sont en équilibre avec le solide.
Je pose pour alléger les notations :
[H3O+]=h et je suppose l'existence du solide.
Tu peux alors exprimer [Zn2+] en fonction de h et de Ks. Tu peux aussi exprimer [Zn(OH)42-] en fonction de h, Ke et  . Tu peux alors exprimer la solubilité s, somme de ces deux concentrations, comme une fonction de h. Tu peux alors calculer la dérivée de s par rapport à h et remplir un tableau de variations comme en maths.
. Tu peux alors exprimer la solubilité s, somme de ces deux concentrations, comme une fonction de h. Tu peux alors calculer la dérivée de s par rapport à h et remplir un tableau de variations comme en maths.
Bonjour, merci pour votre réponse.
Pourriez vous expliquer pourquoi la solubilité est la somme des concentration en ions zinc et en ions Zn(OH)42- quand ces ions sont en équilibre avec le solide ?
La solubilité d'un solide est la quantité maximale que peut dissoudre un litre de solution : c'est donc la quantité dissoute par litre quand la solution est en équilibre chimique avec le solide. Or, la dissolution de Zn(OH)2 produit soit des ions Zn2+ soit des ions Zn(OH)4-2 soit un mélange des deux,selon le pH ; d'où la formule générale de s : somme des deux concentrations.